
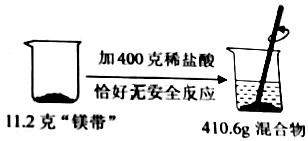
 镁带在空气中易氧化生成氧化镁.某同学为测定某镁带的变质程度.他们用镁带和稀盐酸进行如图实验,请回答下列问题:
镁带在空气中易氧化生成氧化镁.某同学为测定某镁带的变质程度.他们用镁带和稀盐酸进行如图实验,请回答下列问题:分析 (1)镁能与稀盐酸反应放出了氢气,根据质量守恒定律求出生成氢气的质量;
(2)根据氢气的质量求出镁的质量,与镁反应的稀盐酸中溶质的质量,即可计算出“镁带”中单质镁的质量分数;
(3)根据镁的质量求出氧化镁的质量,再根据氧化镁质量求出与氧化镁反应的盐酸中溶质的质量,最后根据溶质分数的计算公式计算即可.
解答 解:(1)由质量守恒定律可知,实验中生成氢气的质量为:11.2g+400g-410.6g=0.6g;
(2)设镁的质量为x,与镁反应的盐酸中溶质的质量为y
Mg+2HCl=MgCl2+H2↑
24 73 2
x y 0.6g
$\frac{24}{x}=\frac{73}{y}=\frac{2}{0.6g}$ 解得:x=7.2g y=21.9g
“镁带”中单质镁的质量分数为:$\frac{7.2g}{11.2g}×100%$≈64.3%
(3)氧化镁的质量为:11.2g-7.2g=4g
设与氧化镁反应的盐酸中溶质的质量为z
MgO+2HCl=MgCl2+H2O
40 73
4g z
$\frac{40}{73}=\frac{4g}{z}$ 解得:z=7.3g
稀盐酸的溶质分数为:$\frac{21.9g+7.3g}{400g}×100%$=7.3%
故答为:(1)0.6;(2)“镁带”中单质镁的质量分数为64.3%;(3)7.3%
点评 本题属于根据化学方程式、溶质质量分数的综合计算,根据质量守恒定律求出氢气的质量是解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 回收利用废旧金属 | B. | 吃经高温蒸煮后的霉变大米 | ||
| C. | 将取出的剩余药品放回原瓶 | D. | 用工厂废水浇灌菜地 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用燃着的木条区分氮气和二氧化碳 | B. | 用肥皂水区分软水和硬水 | ||
| C. | 用闻气味的方法区分白酒和白醋 | D. | 用紫色的石蕊试液区分CO2和CO |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe3+、OH-、Cl- | B. | Ag+、Cl-、NO3- | C. | Cu2+、H+、SO42- | D. | Na+、H+、CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
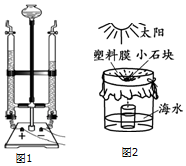 水是重要资源.
水是重要资源.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -1 | B. | +3 | C. | +5 | D. | +7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com