
 Ϊ�˲ⶨij�ֻ�ͭ��ͭ��п�ĺϽ𣩵���ɣ�ȡ�û�ͭ��Ʒ��м100g����400gϡ�����4�μ��뵽����Ʒ�У�������ݼ�¼���±���
Ϊ�˲ⶨij�ֻ�ͭ��ͭ��п�ĺϽ𣩵���ɣ�ȡ�û�ͭ��Ʒ��м100g����400gϡ�����4�μ��뵽����Ʒ�У�������ݼ�¼���±���| ��1�� | ��2�� | ��3�� | ��4�� | |
| ����ϡ����������g�� | 100 | 100 | 100 | 100 |
| ʣ�����������g�� | 87 | 74 | 67.5 | 67.5 |
���� ��1��п��ͭ���ֽ�����ֻ��п�����ᷢ����Ӧ�����ݱ��е����ݿ�֪��ÿ100gϡ���ᷴӦ��п��������13���ݴ˷����ļ���������ʣ�࣮
��2�������μ���������������ټ���˵��п����ȫ��Ӧʣ�����ȫ����ͭ���ɴ������
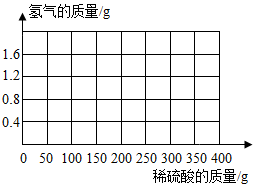
��3������п��������������ɵ����������������ݷ�Ӧ���ɵ��������������ϡ���������Ĺ�ϵ����ͼʾ��
��� �⣺��1��п��ͭ���ֽ�����ֻ��п�����ᷢ����Ӧ���ɱ��е����ݿ�֪��ÿ100gϡ���ᷴӦ��п��������13g���������з�Ӧп��������74g-67.5g=6.5g��13g��˵���˵�3��4����������ʣ�ࣻ
��3���ɱ��е�����֪���������ټ���˵��п����ȫ��Ӧ��ʣ�����ȫ����ͭ����ͭ������Ϊ67.5g�����Ըû�ͭ��Ʒ��ͭ��п��������Ϊ��67.5g����100g-67.5g��=27��13��
��3������������������Ϊx
Zn+H2SO4 �TZnSO4 +H2��
65 2
100g-67.5g x
$\frac{65}{2}=\frac{100g-67.5g}{x}$ ���x=1g
����ȫ��Ӧ�������������y
13g��100g=��100g-67.5g����y ���y=250g��
���ϼ����֪����ȫ��Ӧ�������������250g�����ɵ�������������1g����������Ӧ���ɵ��������������ϡ���������Ĺ�ϵͼ���£�
�ʴ�Ϊ����1��3��4����2��27��13����3������������������1g����Ӧ���ɵ��������������ϡ���������Ĺ�ϵ����ͼ��
���� Ҫ������Ӧ���ɵ��������������ϡ���������Ĺ�ϵͼ���ؼ���Ҫ�ҳ���ȫ��Ӧ����������������ɵ�������������


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����--�������--��ȼ�� | |
| B�� | �ɱ�--�����--�����������ܶȴ��ڿ��� | |
| C�� | ����̿--������о--������ | |
| D�� | ϡ������--���--ͨ���ܷ�����ͬ��ɫ�Ĺ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ�����ʵı�����Һ��һ�������IJ�������Һ��Ũ�ȴ� | |
| B�� | �ڱ�����Һ��ټ����κ����ʶ������ܽ� | |
| C�� | ij������Һ���¶�����ʱ������Һ���������䣬����Һ��Ũϡ�̶�Ҳ���� | |
| D�� | һ���¶��£�������Һ�е����ʺ��ܼ��������Ȳ��Ǹ���ֵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ζ | B�� | �۲���ɫ | ||
| C�� | ��ȼ�ŵ�ľ�����뼯��ƿ�� | D�� | ��������ȼ�պ�IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ���������˵����ʿ������Ӧ�������ĸ�ѡ���У�����Ҫ����ǣ�������
��ͼ���������˵����ʿ������Ӧ�������ĸ�ѡ���У�����Ҫ����ǣ�������| �� | �� | �� | �� | |
| A | Fe2O3 | CO | O2 | C |
| B | HCl | Cu | AgNO3 | Zn |
| C | CaCO3 | HCl | Cu | O2 |
| D | H2 | O2 | Fe | HCl |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
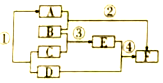 A-F��ʾ���л�ѧ���������ʣ�����֮���ת����ϵ��ͼ��ʾ����Ӧ��������������������ȥ��������A�������ȼ�ϣ�C�����ڳ���Ǧ�������У���Ũ��Һ����ˮ�ԣ�DΪ�������ʣ���Ͻ���ʹ�����Ľ������ϣ�E����Һ����ɫ���Իش��������⣺
A-F��ʾ���л�ѧ���������ʣ�����֮���ת����ϵ��ͼ��ʾ����Ӧ��������������������ȥ��������A�������ȼ�ϣ�C�����ڳ���Ǧ�������У���Ũ��Һ����ˮ�ԣ�DΪ�������ʣ���Ͻ���ʹ�����Ľ������ϣ�E����Һ����ɫ���Իش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com