
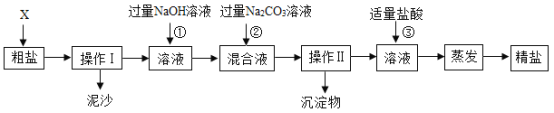
【题目】同规格海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质,为了有效将粗盐提纯,实验的各步操作流程如图所示:
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是_____.
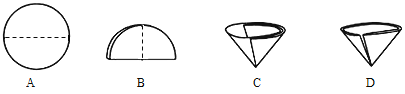
(2)操作Ⅰ和操作Ⅱ的名称是_____,该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是_____(填序号).
(3)在实验过程中加入过量的NaOH溶液①的有关化学方程式是_____.
(4)操作Ⅱ完成后产生的沉淀物的化学式是_____、_____.
(5)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌 外还可采取_____等措施.
(6)判断加入的盐酸“适量”的方法是_____.
(7)实验所得精盐的质量_____(填“大于”、“小于”或“等于”)粗盐中NaCl的质量.
【答案】水 过滤 D MgCl2+2NaOH═Mg(OH)2↓+2NaCl Mg(OH)2 CaCO3 间歇加热 至不再产生气泡为止 大于
【解析】
过滤能够把液体和固体分离;
氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳.
(1)在完成操作Ⅰ之前,必须加入的X物质是水.
故填:水.
(2)操作Ⅰ和操作Ⅱ的名称是过滤,该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D.
故填:过滤;D.
(3)在实验过程中加入过量的NaOH溶液时,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(4)操作Ⅱ完成后产生的沉淀物的化学式是Mg(OH)2、CaCO3.
故填:Mg(OH)2;CaCO3.
(5)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌 外还可采取等措施间歇加热.
故填:间歇加热.
(6)判断加入的盐酸“适量”的方法是至不再产生气泡为止.
故填:至不再产生气泡为止.
(7)实验所得精盐的质量大于粗盐中NaCl的质量这是因为反应生成了氯化钠.
故填:大于.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:初中化学 来源: 题型:
【题目】A~G是初中化学常见的物质,由氢、碳、氧、钙、铁5种元素中的一种或几种组成.物质之间的部分反应及转化关系如图所示,图中“→”表示转化关系,“﹣”表示相互反应.已知A是维持生命活动的气体单质,F是一种红色固体,B、D、E、F都由两种元素组成,C由三种元素组成.
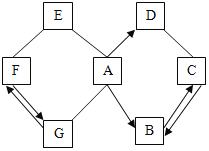
(1)写出相应物质的化学式:A__________;F__________.
(2)B→C的化学方程式为__________.
(3)D、E的化学性质不同的原因是__________.
(4)以下说法不正确的是_____.
①A→D的反应一定是化合反应
②E与F反应过程中各元素化合价均没有改变
③G发生缓慢氧化得到F
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我区某校化学社团﹣﹣“拉瓦锡实验室”的同学们在化学实验室进行了一系列的实验探究活动.
(1)甲组同学的实验是除去粗盐中难溶性杂质,实验步骤主要有四步,如图1.
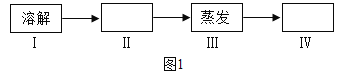
①步骤Ⅲ,给蒸发皿加热时_____(填“需要”或“不需要”)垫石棉网,当出现_____时,停止加热;
②步骤Ⅳ是_____.
(2)乙组同学进行的实验是“从NaCl和Na2CO3的混合物中提纯NaCl”.同学们经过讨论认为利用两物质化学性质的差异,可采用如下化学方法来提纯.
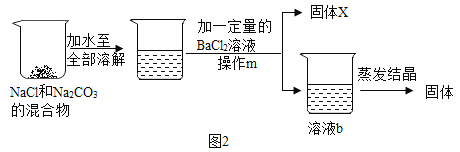
①如图2中X的化学式为_____.由于BaCl2溶液的用量不易控制,会使溶液b的溶质有多种情况,导致蒸发后得到的固体可能不纯.同学们对方案中溶液b的溶质成分进行了猜想.猜想一:NaCl、BaCl2 猜想二:NaCl 猜想三_____;
②经讨论,大家认为只用一种试剂就能判断出溶液b中溶质的成分,这种试剂是_____(写名称)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下图装置进行实验。
内容 装置 | I探究燃烧的条件(已知白磷的着火点为40℃) | II验证使石蕊变色的是碳酸而不是二氧化碳 |
| ①将胶头滴管内吸入约2mL冷水,在分液漏斗内放入约20mL开水。 ②在A管中装入一小块白磷。并塞进橡胶塞。 ③将冷水和开水分别放入A、B支管内。 ④倾斜Y型管,将B中开水倒入A中。 ⑤再次倾斜Y型管,将A中热水(约90℃)倒入B中。 | ①在Y型管的A管中装入用石蕊浸泡的干燥的紫色小花 ②在Y型管的B管中加入适量碳酸钠。 ③将胶头滴管内吸入蒸馏水,塞进橡胶塞。向分液漏斗内注入稀硫酸。 ④…… |
(1)实验I 中发生反应的化学方程式为_____。
(2)实验I中能证明燃烧可燃物温度需要达到着火点的现象是_____。
(3)实验II中B管内将发生反应的化学方程式为_______。
(4)实验II中步骤④的具体操作是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种含CaCO3与CaO的混合物,测得其中钙元素质量分数为50%.取该混合物16g,经高温煅烧后,将剩余固体投入足量水中,固体全部溶解生成Ca(OH)2,则生成的Ca(OH)2质量为( )
A.3.7gB.7.4gC.14.8gD.22.2g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一密闭容器中加入甲、乙、丙、丁四种物质,在下定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示。下列说法中不正确的是
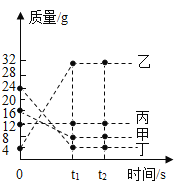
A.该反应为化合反应
B.丙可能为该反应的催化剂
C.该反应中,乙、丁的质量变化之比为7:5
D.该反应中,甲、乙的质量变化之比为1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:①金属钠是一种活泼的金属,与水反应生成氧氧化钠和氢气;②难溶于水的碱受热分解生成相应的氧化物和水。A、B、C、D、E、F、G、H是初中化学中常见的物质,甲、乙、丙是三种金属。其中甲最活泼,乙是红色金属,丙能被磁铁吸引。各物质间相互转化关系如下图:
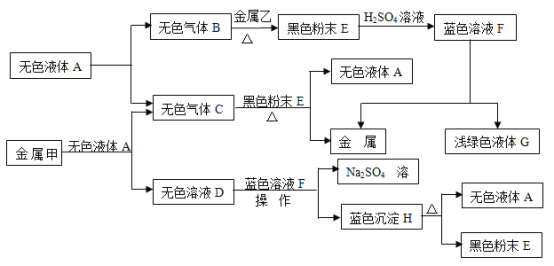
请回答下列问题:
(1)写出A、E、G的化学式:A_____,E_____,G_____。
(2)操作X的名称是______。
(3)①无色溶液D与蓝色溶液F反应的化学方程式为___________;
②金属甲与无色液体A反应的化学方程式为________________________,该反应的基本类型______;
③蓝色沉淀H受热分解反应的化学方程式为______________。
(4)甲、乙、丙三种金属的活动性由强到弱的顺序是_______,无色气体C在点燃或加热前必须进行的操作是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业用石灰石吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙),简易流程如图,主要的反应为:2CaCO3 + O2 + 2SO2 = 2CaSO4 + 2X。
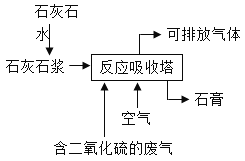
(1)主要反应中物质X的化学式为:___________。
(2)反应前后,硫元素化合价从+4→ __________。
(3)减少二氧化硫的排放,主要为了___________。(填序号)
A减少酸雨形成 B减少温室效应 C防止破坏臭氧层
(4)若处理含有3.2kg二氧化硫的废气,要将其完全吸收,至少需要碳酸钙______kg。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国“青蒿素之母”屠呦呦获2015年诺贝尔生理学或医学奖,屠呦呦发现的青蒿素(青蒿素的化学式:C15H22O5),它是一种用于治疗疟疾的药物,请回答:
(1)青蒿素的相对分子质量为_____.
(2)青蒿素中碳、氢、氧三种元素的质量比为_____
(3)青蒿素中氧元素的质量分数是_____(精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com