
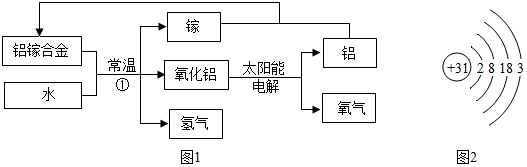
分析 (1)根据合金的硬度大于纯金属的硬度来分析回答;
(2)氢气燃烧只生成水,不污染环境,所以氢能是一种清洁能源;
(3)根据镓在化学反应中所起的作用;化学方程式的书写以及基本反应类型的判断来分析;
根据电解水生成氢气和氧气,然后与镓铝合金制取氢气得出后者制取氢气的优点;
(4)根据镓原子最外层电子数可知,在化学反应中易失去3个电子而显+3价,结合反应实质来分析.
(5)根据水的组成分析回答;
(6)根据物质的变化分析可以循环使用的物质.
解答 解:(1)由于合金的硬度大于纯金属的硬度,所以两块金属片相互刻划后,在铝片上有明显的划痕,说明硬度比合金小;
(2)氢能是一种清洁能源,具有广阔的发展前景;氢气燃烧生成物只有水,不污染环境;
(3)反应①中镓能使该反应在常温下进行,而其质量与化学性质在反应前后没有发生改变,所以反应①中镓充当了催化剂,起到了催化作用;在催化剂的作用下,铝与水反应生成氧化铝和氢气,反应的化学方程式是:2Al+3H3O $\frac{\underline{\;催化剂\;}}{\;}$Al2O3+3H2↑;该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应;电解水制取氢气需要消耗电能且反应的速度慢;镓铝合金制取氢气常温下进行不需要消耗能源,反应速度较快;
(4)镓显+3价,镓与稀盐酸反应生成氯化镓和氢气,反应的化学方程式是:2Ga+6HCl=2GaCl3+3H2↑;
(5)由于水中氢、氧元素的质量比是1:8.由质量守恒定律可知,该工艺流程中产生的氢气与氧气的质量比为1:8.
(6)由整个流程中物质的变化可知,可以循环使用的物质是:镓和铝.
故答为:(1)镓合金的硬度大;(2)燃烧的产物是水,无污染;(3)催化作用,2Al+3H3O $\frac{\underline{\;催化剂\;}}{\;}$Al2O3+3H2↑置换反应,常温下反应,节约能源;(4)2Ga+6HCl=2GaCl3+3H2↑;(5)1:8;(6)镓和铝.
点评 本题考查了工艺中的信息给予题,难度不大,注意从题目中获取相关的信息并结合相关的知识分析判断得出结论即可,难度不大,可以考查学生的知识迁移能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
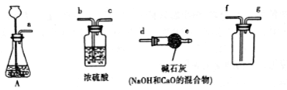 如图是初中化学常见的实验装置图,请回答下列问题.
如图是初中化学常见的实验装置图,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 甲 | 乙 | 丙 | |
| 烧杯+稀盐酸质量 | 130g | 120g | 120g |
| 加入大理石样品的质量 | 20g | 24g | 20g |
| 充分反应后,烧杯+剩余物质量 | 146.7g | 140.7g | 136.7g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
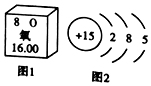 请从微观角度解释下列问题.
请从微观角度解释下列问题.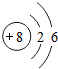 .
.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
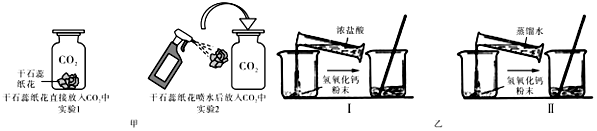
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由氢、氧两种元素组成的 | |
| B. | 水的蒸发和水的通电分解都可说明分子可分 | |
| C. | 用食盐水可鉴别硬水和软水 | |
| D. | 水沸腾时可冲起壶盖说明温度升高分子会变大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com