
分析 原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字.
元素符号可表示一种元素、一个原子.
解答 解:由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2O可表示2个氧原子.
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故2Mg2+可表示2个镁离子.
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则2H2O可表示2个水分子.
元素符号可表示一种元素、一个原子,N可表示氮元素、1个氮原子.
故答案为:2个氧原子;2个镁离子;2个水分子;氮元素、1个氮原子.
点评 本题难度不大,掌握常见化学用语(元素符号、原子符号、分子符号、离子符号等)的书写方法是正确解答此类题的关键.


科目:初中化学 来源: 题型:计算题
| 实验次数 | 一 | 二 | 三 |
| 稀盐酸质量(克) | 40 | 60 | 40 |
| 样品质量(克) | 17 | 17 | 30 |
| 剩余物质质量(克) | 50.4 | 70.4 | 63.4 |
| 产生气体的质量(克) | 6.6 | a | 6.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1g水和1g酒精混合后总质量等于2g | |
| B. | 1L水和1L酒精混合后总体积小于2L | |
| C. | 1g硫与1g氧气恰好完全反应可生成2g二氧化硫 | |
| D. | 1g碳与1g氧气恰好完全反应可生成2g二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
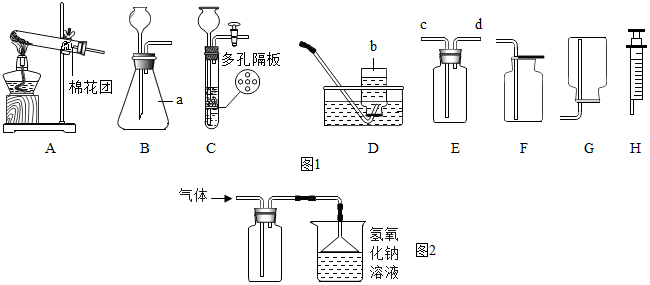
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com