现有一包含有氯化钠和碳酸钠的固体化合物,为测定其成分,取一定质量的化合物于试管中,加入103g稀盐酸,恰好完全反应,生成的气体全部逸出,得到4.4g气体.将所得溶液冷却至t℃,恰好成为该温度下的饱和溶液,经测定溶液中的溶质含钠元素的质量为13.8g.求反应后所得溶液中溶质的质量分数.(最后计算结果精确到0.1%)
解:设碳酸钠的质量为x,生成氯化钠的质量为y,所得溶液中溶质的质量为z.
Na
2CO
3+2HCl═2NaCl+H
2O+CO
2↑
106 117 44
x y 4.4g

=
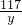
=

解得:x=10.6g,y=11.7g
设反应后的溶液中氯化钠的质量为z,则根据钠元素的质量守恒可得:
Na~NaCl
23 58.5
13.8g z

=

解得:z=35.1g
原混合物中NaCl的质量为:35.1g-11.7g=23.4g
所得溶液的质量为:23.4g+10.6g+103g-4.4g=132.6g;
所得溶液中溶质的质量分数为:
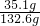
×100%=26.5%;
答:所得溶液中溶质的质量分数为26.5%.
分析:根据溶液中溶质的质量分数计算方法可以知道,欲求反应后所得溶液中溶质的质量分数,必须先求出溶液的质量和溶质的质量,根据题给条件可以知道应该先计算出加入的固体的质量,而溶液中溶质的质量可以根据钠元素的质量守恒计算出来,进而求出其溶液中溶质的质量分数即可.
点评:此题是对化学方程式以及溶液相关问题的考查,利用质量守恒定律,计算出反应后溶液的质量是解决问题的关键.

 =
=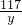 =
=
 =
=
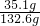 ×100%=26.5%;
×100%=26.5%;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案