
科目:初中化学 来源: 题型:选择题
| A. | 物质溶解往往伴随有能量的变化 | |
| B. | 铝比铁具有更好的抗腐蚀性能,是因为铁比铝更活泼 | |
| C. | 建造游泳中心“水立方”用到的聚乙烯是有机合成材料 | |
| D. | 用汽油和加了洗涤剂的水分别除去衣服上的油污,两者去污原理不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在实验探究课上,化学老师给大家的是“贝贝熊暖贴”.它是一种一次性取暖片.它的填充物的主要成分是什么?这个问题引起了同学们的好奇.剪开内包装,倒出其中的粉末,发现呈黑色.老师告诉大家,黑色粉末里含有活性炭、铁粉、氧化铜中的一种或几种.请你一起参与同学们的探究:
在实验探究课上,化学老师给大家的是“贝贝熊暖贴”.它是一种一次性取暖片.它的填充物的主要成分是什么?这个问题引起了同学们的好奇.剪开内包装,倒出其中的粉末,发现呈黑色.老师告诉大家,黑色粉末里含有活性炭、铁粉、氧化铜中的一种或几种.请你一起参与同学们的探究:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 相对分子质量为282 | |
| B. | 其中氢元素的质量分数最大 | |
| C. | 其中碳、氢、氧三种元素的质量比为90:11:40 | |
| D. | 每个分子中含有15个碳原子,22个氢原子和5个氧原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用金属来制作炊具,是利用了其化学性质 | |
| B. | 自然界的水都或多或少含有杂质,所以最健康的饮用水就是蒸馏水 | |
| C. | 空气中含有的元素质量分数最大的是氧 | |
| D. | 地表上能够以游离态存在的金属元素只能是很不活泼的少数几种 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  | 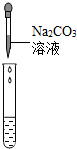 | 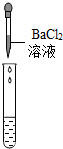 |
| 实验现象 | 试纸变色,对比比色卡,pH=1 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com