
 如图是CuSO4等五种物质的部分相互转化关系图,其中A、B、C、D是初中化学常见的不同类别的物质(酸、碱、盐和单质),B有两种元素组成,C是一种钠盐,D含有钙元素,“-”表示相连的两种物质能发生反应.
如图是CuSO4等五种物质的部分相互转化关系图,其中A、B、C、D是初中化学常见的不同类别的物质(酸、碱、盐和单质),B有两种元素组成,C是一种钠盐,D含有钙元素,“-”表示相连的两种物质能发生反应.分析 根据CuSO4等五种物质的部分相互转化关系图,A、B、C、D是初中化学常见的不同类别的物质,B有两种元素组成,C是一种钠盐,D含有钙元素,D会与硫酸铜反应,所以D是氢氧化钙,C会与氢氧化钙反应,所以C是碳酸钠,B会与碳酸钠反应,所以B是盐酸,A是铁,然后将推出的物质进行验证即可.
解答 解:(1)CuSO4等五种物质的部分相互转化关系图,A、B、C、D是初中化学常见的不同类别的物质,B有两种元素组成,C是一种钠盐,D含有钙元素,D会与硫酸铜反应,所以D是氢氧化钙,C会与氢氧化钙反应,所以C是碳酸钠,B会与碳酸钠反应,所以B是盐酸,A是铁,经过验证,推导正确,所以B是盐酸,C是碳酸钠;
(2)通过推导可知,D是氢氧化钙,俗称熟石灰,可以用来改良酸性土壤;
(3)通过推导可知,A会置换出铜,所以A比银活泼;
(4)C与D的反应是氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,该反应属于复分解反应.
故答案为:(1)盐酸,碳酸钠;
(2)熟石灰,改良酸性土壤;
(3)强;
(4)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,复分解.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


科目:初中化学 来源: 题型:选择题
| A. | H、O原子个数比为1:8 | B. | 相对分子质量为180 | ||
| C. | 阿司匹林中含21种元素 | D. | 氧元素的质量分数最小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
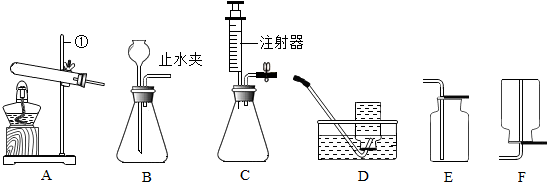
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(杂质) | 操作方式 |
| A | H2(水蒸气) | 通过装有浓硫酸的洗气瓶 |
| B | CO(O2) | 缓慢通过灼热铜网 |
| C | NaCl溶液(Na2CO3) | 滴加盐酸至恰好不再产生气泡为止 |
| D | CaCl2溶液(HCl) | 加入足量CaCO3固体充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com