
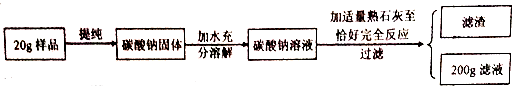
分析 碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)20g样品中碳酸钠的质量为:20g×53%=10.6g,
答:20g样品中碳酸钠的质量为10.6g.
(2)设反应生成氢氧化钠质量为x,
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,
106 80
10.6g x
$\frac{106}{10.6g}=\frac{80}{x}$,
x=8g,
反应后所得滤液中氢氧化钠的质量分数为:$\frac{8g}{200g}$×100%=4%,
答:反应后所得滤液中氢氧化钠的质量分数为4%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 硫酸 | B. | 硫酸铜和硫酸亚铁 | ||
| C. | 硫酸铜 | D. | 只有硫酸亚铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学兴趣小组为研究氢氧化钠的化学性质,进行如下实验.
化学兴趣小组为研究氢氧化钠的化学性质,进行如下实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CaCO3(CaO) | 无 | 高温 |
| B | H2O(植物油) | 洗涤剂 | 振荡、搅拌 |
| C | CuO(铜粉) | 足量氧气 | 灼烧 |
| D | KCl(KClO3) | 二氧化锰 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题

| A. | 钾原子的核电荷数为19 | B. | 钾离子的符号为K+ | ||
| C. | 钾的相对原子质量为39.10g | D. | 化学反应中,钾原子易得电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铅锑合金熔点高,因此被用于制作保险丝 | |
| B. | 铵态氮肥不能与草木灰混合使用,是因为二者反应会降低肥效 | |
| C. | 街道上的路灯同时亮,同时灭,是由于它们的连接方式是并联 | |
| D. | 充电宝插在插座上充电时,将电能转化为化学能 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水时,电极两端有气泡产生,生成氢气和氧气的体积比为2:1 | |
| B. | 加热通入足量二氧化碳后的石蕊溶液;溶液由红色变为紫色 | |
| C. | 硫在空气中燃烧:发出蓝紫色火焰,产生有刺激性气味的气体,放热 | |
| D. | 单质碳还原氧化铁:红棕色固体变成银白色,生成的气体能使澄清石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
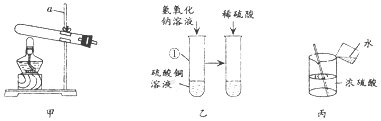
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
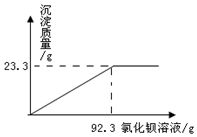 某硫酸铵[(NH4)2SO4]样品,可能含有少量的氯化铵[NH4Cl],为了测定硫酸铵样品中硫酸铵的质量分数,取样品16.0g,加入40.0g水中完全溶解后,向溶液中加入某种质量分数的氯化钡溶液,实验中精确测得产生白色沉淀的质量与加入氯化钡溶液的质量的关系如图所示.
某硫酸铵[(NH4)2SO4]样品,可能含有少量的氯化铵[NH4Cl],为了测定硫酸铵样品中硫酸铵的质量分数,取样品16.0g,加入40.0g水中完全溶解后,向溶液中加入某种质量分数的氯化钡溶液,实验中精确测得产生白色沉淀的质量与加入氯化钡溶液的质量的关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com