
分析 (1)根据常用仪器的名称和用途判断;
(2)实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,并据二氧化碳的密度和溶解性选择收集装置,依据反应原理书写方程式;
(3)依据反应物的状态和条件选择发生装置,收集较纯净的气体用排水法;
(4)用加热熟石灰和氯化铵固体来制取氨气,属于固体加热型,故选发生装置A,氨气密度比空气小,极易溶于水,据反应原理书写方程式..
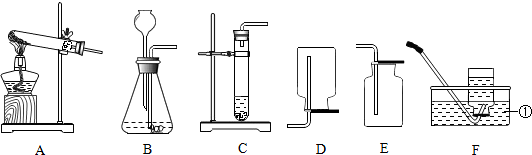
解答 解:(1)根据常用仪器的名称和用途判断可知标号仪器是水槽;
(2)实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,可用BC制取,而B中长颈漏斗未伸入液面以下,气体会从漏斗逸出,所以不可用,选择发生装置C;二氧化碳的密度比空气大,能溶于水,可用向上排空气法收集,大理石主要成分碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)实验室用若用高锰酸钾制取并收集较纯净的氧气,属于固体加热型,故选发生装置A,氧气不易溶于水,所以收集较纯净的氧气可用排水法;
(4)实验室用氯化铵固体与碱石灰固体共热来制取氨气,属于“固体加热型”,故选择A装置,氨气的相对分子质量是14+3=17<29,密度比空气小,所以可用向下排空气法收集,极易溶于水,不能用排水法收集,氯化铵(NH4C1)和氢氧化钙粉末两种固体的混合物,反应条件是加热,生成物是氯化钙和水以及氨(NH3),方程式是:2NH4C1+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
故答案为:
(1)水槽;
(2)C;E;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)AF;
(4)A;D;2NH4C1+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
点评 解题时明确依据反应物的状态和条件选择发生装置,根据气体的密度和溶解性选择收集装置,并正确书写方程式.


科目:初中化学 来源: 题型:多选题
| A. | 肥皂水pH=10 | B. | 纯碱溶液pH=7 | C. | 食醋溶液 pH=9 | D. | 橘子汁pH=4 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 人体中含量最多的金属元素是Ca | |
| B. | 日常生活中应用最广泛,目前世界上产量最高的金属是Fe | |
| C. | 地壳中含量最多的金属元素是Fe | |
| D. | 导电性最好的金属是Ag |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 大于12 mL | B. | 等于12 mL | C. | 小于12 mL | D. | 以上都不对 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com