
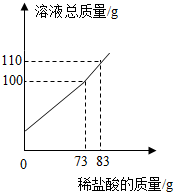
 某纯碱样品中含少量氯化钠,称取11g样品于烧杯中,加20.4g的水将其全部溶解,再逐滴加入一定质量分数的稀盐酸并振荡,实验过程中,测得加入稀盐酸的质量和溶液总质量的关系如图所示,计算(写出计算过程):
某纯碱样品中含少量氯化钠,称取11g样品于烧杯中,加20.4g的水将其全部溶解,再逐滴加入一定质量分数的稀盐酸并振荡,实验过程中,测得加入稀盐酸的质量和溶液总质量的关系如图所示,计算(写出计算过程):分析 (1)根据质量守恒定律计算生成二氧化碳的质量;
(2)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,依据二氧化碳的质量计算参加反应的碳酸钠的质量,然后计算质量分数.
解答 解:(1)根据质量守恒定律,反应后溶液减少的质量就是反应中生成的二氧化碳的质量为:11+73+20.4-100=4.4g;
(2)设参加反应的碳酸钠的质量是x
Na2C03+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$
x=10.6g
碳酸钠的质量分数为:$\frac{10.6g}{11g}$×100%=96.4%.
故答案为:(1)4.4g;
(2)碳酸钠的质量分数为96.4%.
点评 本题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用反应前后物质质量的变化求出生成二氧化碳的质量,而后根据它的质量求出其它的需要的物质的质量解答即可.


科目:初中化学 来源: 题型:解答题
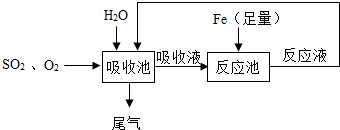 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
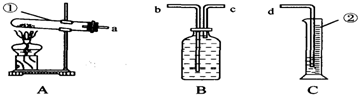
 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:| 实验操作 | 实验现象 |
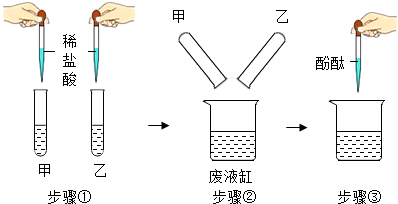 | 步骤①:甲溶液中观察到现象A, 乙溶液中无明显现象 步骤②:底部有白色沉淀 步骤③:上层为无色透明的溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用氢氧化钠溶液清洗盛装过植物油的瓶子 | |
| B. | 用酒精或汽油清洗掉衣服上的油污 | |
| C. | 用稀盐酸清洗盛装过石灰水的试剂瓶 | |
| D. | 加了餐具洗洁精的热水洗涤碗碟上的油污 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 焚烧秸秆,增加肥力 | B. | 禁用农药,保护水资源 | ||
| C. | 回收塑料,再生减污 | D. | 深埋电池,消除污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可燃冰能燃烧是因为其主要成分是甲烷 | |
| B. | 泡沫灭火器可用于扑灭电器引起的失火 | |
| C. | 雨水呈酸性的雨就是酸雨 | |
| D. | C02、CO、N02、S02都是有毒有害气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
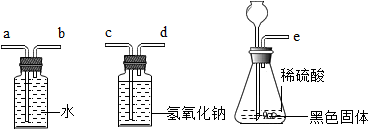 课外小科约老师继续探究铁粉和硫粉反应的实验:他们各自取一定量的铁粉和硫粉均匀混合后堆放在石棉网上,在其中插入烧红的玻璃棒,反应立即发生.拿掉玻璃棒后,反应继续剧烈进行,反应过程中有少量刺激性气味的气体X产生.反应结束后,都得到了黑色固体.老师得到的黑色固体不会被磁铁吸引,而小科的却会被磁铁吸引.
课外小科约老师继续探究铁粉和硫粉反应的实验:他们各自取一定量的铁粉和硫粉均匀混合后堆放在石棉网上,在其中插入烧红的玻璃棒,反应立即发生.拿掉玻璃棒后,反应继续剧烈进行,反应过程中有少量刺激性气味的气体X产生.反应结束后,都得到了黑色固体.老师得到的黑色固体不会被磁铁吸引,而小科的却会被磁铁吸引.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com