
 ����һ�����еĻ�ѧ��ȤС���ͬѧ������ͼ��ʾװ�ý������÷ֽ���������ȡ��
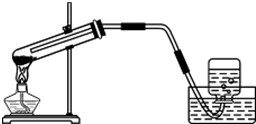
����һ�����еĻ�ѧ��ȤС���ͬѧ������ͼ��ʾװ�ý������÷ֽ���������ȡ������ ��1��������ѧ֪ʶ������ȡ�����ķ������з�����
��2��������ȡ����ķ���װ���е��ܲ������̫��������������ĵ��������ȹ���ҩƷʱ�Թܿ�Ӧ������б����ֹ����ˮ�������Թܵײ��������Թ�ը�ѣ����ȸ��������ȡ�������Թܿ�Ӧ��һ��������ֹ����ʱ������ط�ĩ���뵼�ܽ��з�����
��3�����ݸ��������ȡ��������ˮ���ռ����������ȵͣ��������ռ�ʱ�̹��磬Ҳ�����Ǽ���ƿû��װ��ˮ���з�����
��4���ٸ��������غ㶨�ɼ�������������������
�ڸ��������������������ĸ�����ص�������Ȼ�����ʣ�������ص�������
��� �⣺��1��ͨ��ѧϰ��֪����ȡ�����ķ������з���Һ̬��������������غͶ������̵Ļ����ȣ�
��2����ȡ����ķ���װ���е��ܲ������̫��������������ĵ��������ȹ���ҩƷʱ�Թܿ�Ӧ������б����ֹ����ˮ�������Թܵײ��������Թ�ը�ѣ����ȸ��������ȡ�������Թܿ�Ӧ��һ��������ֹ����ʱ������ط�ĩ���뵼�ܣ�����ͼ��װ����3�����ԵIJ��㣻
��3�����������ȡ��������ˮ���ռ����������ȵͣ��������ռ�ʱ�̹��磬Ҳ�����Ǽ���ƿû��װ��ˮ����ѡ��CD��
��4��������������������12g-11.36g=0.64g��
�����ĸ�����ص�����Ϊx��
2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2��
316 32
x 0.64g
$\frac{316}{x}$=$\frac{32}{0.64g}$
x=6.32g
����ʣ�������ص�����Ϊ��12g-6.32g=5.68g��
�ʴ�Ϊ����1������Һ̬��������������غͶ������̵Ļ���
��2��3��
��3��CD��
��4����0.64g��
��5.68g��
���� ������Ҫ���鳣������ķ���װ�����ռ�װ�õ�̽��������װ�����ݷ�Ӧ���״̬�ͷ�Ӧ����ѡ���ռ�װ������������ܶȺ��ܽ���ѡ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ó���ʯ��ˮ����CO��CO2 | |
| B�� | �ö������̼������������Һ��ˮ | |
| C�� | �ô����ǵ�ľ������CO2��N2 | |
| D�� | ����ɫʯ����Һ�������Ͷ�����̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
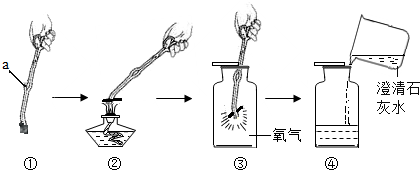
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ����̼���⡢������Ԫ�� | B�� | һ����̼����Ԫ�أ����ܺ���Ԫ�� | ||
| C�� | һ����̼����Ԫ�أ�������Ԫ�� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com