
| 物质质量 | 第1次 | 第2次 | 第3次 |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀盐酸的质量/g | 120 | 160 | 100 |
| 充分反应后,剩余物总质量/g | 144.6 | 184.6 | 149.6 |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:不详 题型:计算题
| 时间/min | 0 | 3 | 6 | 9 |
| 粗锌及溶液总质量/g | 150.4 | 150.2 | 150.0 | 150.0 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
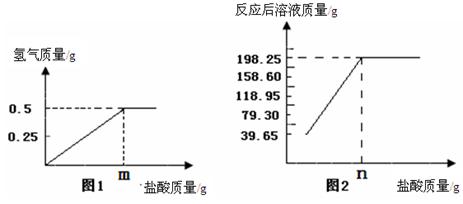

查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| | 甲 | 乙 | 丙 |
| 加入NaOH溶液的质量(g) | 35.0 | 40.0 | 45.0 |
| 反应得到沉淀的质量(g) | 2.5 | 2.9 | 2.9 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| ××牌口服液 主要成分:葡萄糖酸锌 化学是:C12H22O14Zn 每只口服液含葡萄糖酸锌45.5mg ××制药厂 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
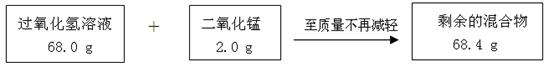
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 次数 | 1 | 2 | 3 | 4 |
| 加入Ca(OH)2溶液的质量/克 | 100 | 100 | 100 | 100 |
| 烧杯中生成沉淀的质量/克 | 1 | m | 3 | 3 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com