
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子.
”表示氧原子.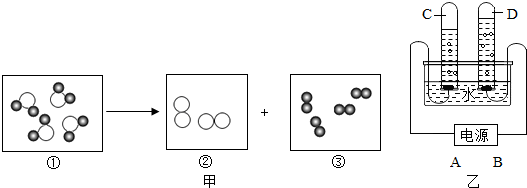
分析 (1)过滤可以把不溶于水的杂质除去;除去水中过多的钙、镁离子可以降低水的硬度;根据化学方程式、质量守恒定律可以判断物质的化学式.
(2)联系电解水的实验进行分析、判断,从而得出正确的结论.
(3)依据反应物、生成物、反应条件书写方程式.
解答 解:(1)除去水样中难溶性固体杂质的操作是过滤;过滤操作中用到的玻璃仪器有漏斗、玻璃棒、烧杯;
加热煮沸时,水中的钙离子能够以碳酸钙的形式从水中析出,镁离子能够以氢氧化镁的形式从水中析出,从而降低水的硬度.由Ca(ClO)2+X+H2O=CaCO3↓+2HClO可知,每个X中含有一个碳原子和两个氧原子,是二氧化碳,化学式是CO2.
故答案为:过滤;漏斗;煮沸;CO2.
(2)化合物是纯净物,所以化合物中只有一种分子,且分子中含有多种原子,分析图示中分子的情况可知构成化合物分子的是图①;③所代表的物质是由分子构成,是每个分子由两个氢原子构成的氢分子,氢分子构成氢气,氢气多,大约是氧气体积的2倍,是在负极得到的;
故答案为:①;C;负.
(3)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气,反应的化学方程式是:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑;
故答案为:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑.
点评 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:初中化学 来源: 题型:多选题
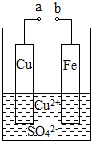 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成棕黄色 | |
| D. | a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
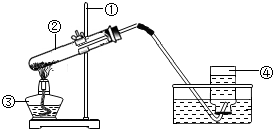 (1)指出下面实验室用高锰酸钾制取氧气的装置图中的四处错误:
(1)指出下面实验室用高锰酸钾制取氧气的装置图中的四处错误:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验次数 项目 | 第一次 | 第二次 | 第三次 | 第四次 |
| 所取石灰石样品的质量/g | 12 | 12 | 12 | 12 |
| 所加稀盐酸的质量/g | 25 | 35 | 50 | 70 |
| 生成二氧化碳气体的质量/g | 2.2 | 3.1 | 4.4 | 4.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com