
| 地 区 | 风景区 | 居民区 | 工厂区 |
| S02的浓度限值( mg/L) | 0.00015 | 0.00050 | 0.00070 |
分析 过滤可以把不溶于水的物质从溶液中分离出来;
硫酸钠和氯化钡反应生成白色沉淀硫酸钡和氯化钠;
根据元素的转化关系可以判断相关方面的问题;
根据提供的数据可以进行相关方面的计算,进一步可以判断相关方面的问题.
解答 解:(1)操作1的名称为过滤,加入过量BaCl2溶液的原因是使硫酸钠完全反应,流程图中,硫酸钠和氯化钡反应生成硫酸钡和氯化钠,发生反应的化学方程式为:
BaCl2+Na2SO4═BaSO4↓+2NaCl.
故填:过滤;使硫酸钠完全反应;BaCl2+Na2SO4═BaSO4↓+2NaCl.
(2)因为二氧化硫中的硫元素完全转化到硫酸钡中,所以BaS04中硫元素的质量为0.165mg时,可以确定S02中硫元素的质量也为0.165mg.
故填:二氧化硫中的硫元素完全转化到硫酸钡中.
(3)设二氧化硫的质量为x,
根据题意有:x×$\frac{32}{64}$×100%=0.165mg,
x=0.33mg,
故填:0.33.
(4)该工厂区大气中S02的含量为:$\frac{0.33mg}{250L}$=0.00132mg/L,
对照空气质量标准可知,该工厂区大气中S02的含量超标.
故填:超标.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
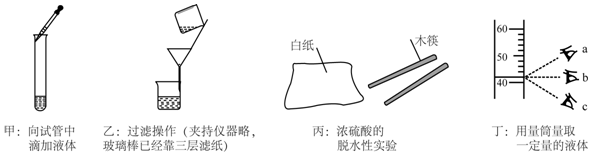
| A. | 向试管中滴加液体,正确的基本操作应如图甲所示,这样可保证将液体滴入试管 | |
| B. | 按图乙所示进行过滤操作,玻璃棒的倾斜角度不合适,这样很可能使液体外漏 | |
| C. | 如图丙所示,浓硫酸使白纸、木筷变黑,是因为浓硫酸吸收了纸和木筷中的水 | |
| D. | 图丁所示的三次读数,a为俯视,b读数方法正确,c的读数比实际液体体积大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | M中只有一种溶质的有(1)和(3) | |
| B. | M中有两种溶质的只有(4) | |
| C. | (1)中的V(A)和(2)、(3)、(4)图中显示的V(B)是相等的 | |
| D. | 当加入盐酸至不再产生气体时,所得溶液中溶质的质量相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二 不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 先无变化后有气泡产生 | 猜想三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com