
分析 (1)根据浓硫酸具有强烈的腐蚀性进行分析解答.
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(3)盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应;通常制作氯化锌用盐酸;除杂不得引入新的杂质.
解答 解:(1)浓硫酸具有吸水性,在实验室常用作干燥剂.
(2)①铁能与稀硫酸发生置换反应,生成氢气和硫酸亚铁,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
②稀硫酸与碳酸钠溶液反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
③硫酸与氯化钡反应生成硫酸钡沉淀和氯化氢,化学方程式为:H2SO4+BaCl2═BaSO4↓+2HCl.该反应是硫酸的特性反应,不属于共性;
(3)①盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应,都能用于金属表面除锈,故选项错误.
②制造药物氯化锌中含有氯元素,盐酸含氯元素,硫酸不含氯元素,故不能用硫酸代替盐酸,故选项正确.
③NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故不能用硫酸代替盐酸,故选项正确.
故答案为:
(1)吸水性;
(2)①Fe+H2SO4=FeSO4+H2↑;
②Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
③H2SO4+BaCl2═BaSO4↓+2HCl;③;
(3)①
点评 本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)、酸的用途等并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
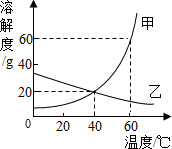 如图是甲、乙两种物质的溶解度曲线,则下列叙述正确的是( )
如图是甲、乙两种物质的溶解度曲线,则下列叙述正确的是( )| A. | 可用100g水配制60℃时溶液质量为180g的甲溶液 | |
| B. | 40℃时,甲、乙两物质溶液的溶质质量分数一定相等 | |
| C. | 升高温度可以将乙的饱和溶液转化为不饱和溶液 | |
| D. | 50℃时,甲物质的溶解度大于乙物质的溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用湿润的pH试纸测量某溶液的pH值 | |
| B. | 欲配制质量分数为10%的CuSO4溶液,将10gCuSO4•5H2O溶解在90g水中 | |
| C. | 用玻璃棒搅拌漏斗中的液体以加快过滤速度 | |
| D. | 实验室不能用排空气法收集CO,但可用排水法收集 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu(NO3)2和HCl | B. | NaOH和BaCl2 | C. | KOH和Mg(NO3)2 | D. | Zn(NO3)2和Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
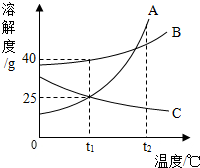 小明同学绘制了A、B、C三种固体物质的溶解度曲线如图.
小明同学绘制了A、B、C三种固体物质的溶解度曲线如图.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeTiO3中Ti的化合价为+3 | B. | X是Ti | ||
| C. | FeTiO3中Ti的化合价为+4, | D. | X是Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com