
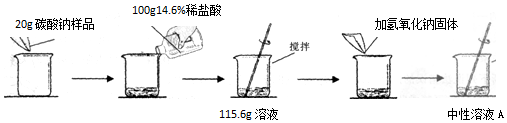
分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断;
稀释溶液时,溶质质量不变.
解答 解:(1)需要36.5%的浓盐酸的质量为:100g×14.6%÷36.5%=40g,
则需要水的质量为:100g-40g=60g,
故填:60g.
(2)样品中碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)设碳酸钠质量为X,反应的氯化氢质量为Y,生成氯化钠质量为Z,
反应生成二氧化碳质量为:20g+100g-115.6g=4.4g,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 73 117 44
X Y Z 4.4g
$\frac{106}{X}$=$\frac{73}{Y}$=$\frac{117}{Z}$=$\frac{44}{4.4g}$,
X=10.6g,Y=7.3g,Z=11.7g,
故填:$\frac{106}{X}$=$\frac{44}{4.4g}$.
(4)该样品中碳酸钠的质量分数为:$\frac{10.6g}{20g}$×1005=53%,
故填:53%.
(5)设氢氧化钠质量为x,生成氯化钠质量为y,
和氢氧化钠反应的氯化氢质量为:100g×14.6%-7.3g=7.3g
NaOH+HCl═NaCl+H2O,
40 36.5 58.5
x 7.3g y
$\frac{40}{x}$=$\frac{36.5}{7.3g}$=$\frac{58.5}{y}$,
x=8g,y=11.7g,
中性溶液A中氯化钠质量为:20g-10.6g+11.7g+11.7g=32.8g,
向中性溶液A中加入76.4g水,最终得到溶液质量为:115.6g+8g+76.4g=200g,
溶质质量分数是:$\frac{32.8g}{200g}$×100%=16.4%,
故填:16.4%.
(6)20t样品中碳酸钠质量为:20t×$\frac{10.6g}{20g}$×100%=10.6t,
设转化成氢氧化钠的质量为z,
Na2CO3~2NaOH,
106 80
10.6t z
$\frac{106}{10.6t}$=$\frac{80}{z}$,
z=8t,
若将20t样品中的纯碱转化为烧碱,则制得含杂质的烧碱质量为:20t-10.6t+8t=17.4t,
答:若将20t样品中的纯碱转化为烧碱,则制得含杂质的烧碱质量为17.4t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 每课必练系列答案
每课必练系列答案科目:初中化学 来源: 题型:推断题
 如图表示的是初中几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为大理石的主要成分,D、E、H是同种类别的物质,请回答以下问题:
如图表示的是初中几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为大理石的主要成分,D、E、H是同种类别的物质,请回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 6.4g | B. | 8g | C. | 10.5 g | D. | 12.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 20℃ | 40℃ | |
| 水 | 109g | 129g |
| 酒精 | 17.3g | 40g |
| A. | 温度和溶剂种类对NaOH的溶解度都有影响 | |
| B. | NaOH易溶于水,也易溶于酒精 | |
| C. | 40℃,40gNaOH溶解在l00g酒精中达到饱和 | |
| D. | 将等质量40℃的饱和NaOH水溶液和饱和NaOH酒精溶液降温至20℃,析出的晶体前者比后者多 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH | B. | NaHCO3 | C. | H2SO4 | D. | K2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com