
| A. | 物质与氧气反应时都会燃烧 | |
| B. | 用木材引燃煤,是为了提高煤的着火点 | |
| C. | 只要温度达到着火点,物质就会燃烧 | |
| D. | 增大可燃物与空气的接触面积,可使其充分燃烧 |
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:解答题
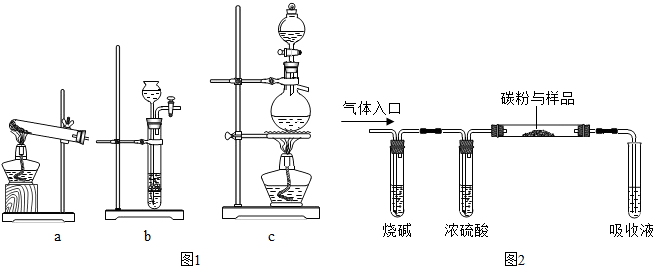
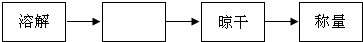
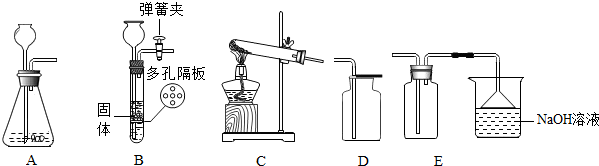
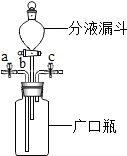 如图所示是实验室常见的装置(a、c为止水夹,b为分液漏斗活塞),利用该装置与其它装置组合,克完成以下实验.
如图所示是实验室常见的装置(a、c为止水夹,b为分液漏斗活塞),利用该装置与其它装置组合,克完成以下实验.| 制取气体 | 装置中应加入的试剂 | 广口瓶中发生反应的化学方程式 | |
| 分液漏斗 | 广口瓶 | ||
| O2 | MnO2 | ||
| CO2 | CaCO3 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
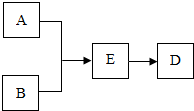 A、B、D、E是初中化学常见物质,分别由C、H、O、S、Ca、Fe等七种元素中的一种或几种组成,四种物质的转化关系如图所示,其中D在常温下为一种生命活动不可或缺的无色液体.其中“→”表示转化关系.
A、B、D、E是初中化学常见物质,分别由C、H、O、S、Ca、Fe等七种元素中的一种或几种组成,四种物质的转化关系如图所示,其中D在常温下为一种生命活动不可或缺的无色液体.其中“→”表示转化关系.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
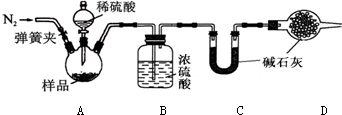
| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少量样品,加水. | 样品全部溶解 | |
| Ⅱ.取溶液于试管中,滴入足量的CaCl2溶液,过滤. | 产生白色沉淀 | 溶液中含有K2CO3. |
| Ⅲ.取Ⅱ所得的滤液于另一试管中,滴加无色酚酞试液. | 酚酞试液变红色 | 溶液中含有KOH. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
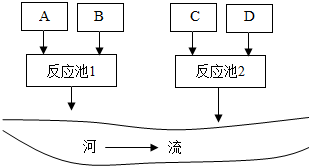 某化学试剂厂A,B,C,D四个车间排放的废水中,分别含有氢氧化钠、硫酸铜、碳酸钠、硫酸中的一种,在不加其他试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流.如图所示:
某化学试剂厂A,B,C,D四个车间排放的废水中,分别含有氢氧化钠、硫酸铜、碳酸钠、硫酸中的一种,在不加其他试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流.如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com