
【题目】2019年1月11日中国国家航天局宣布,中国探月工程嫦娥四号任务圆满成功。
(1)2018年12月8日,嫦娥四号探测器由长征三号乙运载火箭成功发射。运载火箭第一级和第二级的燃料是偏二甲肼(C2H8N2),助燃剂是N2O4,两者反应的化学方程式为![]() ,其中X的化学式为_______________。
,其中X的化学式为_______________。
(2)嫦娥四号使用了大量铝合金,铝不仅密度小,耐腐蚀能力也较强,铝的耐腐蚀能力较强的原因是______。
(3)嫦娥四号上国旗的材料是用聚酰亚胺制成的,聚酰亚胺属于____________(填“天然高分子材料”、“合成高分子材料”或“金属材料”)。
(4)南昌凯迅光电有限公司生产的高效砷化镓太阳能电池外延片用于装备嫦娥四号。已知镓在周期表中信息及其原子结构示意图如图所示,下列说法正确的是_____________。
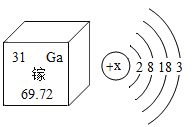
A镓原子核内电子数为31
B镓的相对原子质量为69.72 g
C图中x=31
D镓在化学反应中易得到电子
【答案】![]() 铝与氧气反应在铝的表面形成一层致密的氧化物薄膜 合成高分子材料 C
铝与氧气反应在铝的表面形成一层致密的氧化物薄膜 合成高分子材料 C
【解析】
(1)由题意偏二甲肼(C2H8N2)与助燃剂是N2O4反应的化学方程式为![]() ,根据方程式可知反应物的分子中一共有2个碳原子、8个氢原子、6个氮原子和8个氧原子,生成物分子中有2个碳原子、6个氮原子、4个氧原子和4个X分子,根据质量守恒定律反应前后原子的种类和数目保持不变可知4个X分子中应该含有8个氢原子和4个氧原子,则X的化学式为
,根据方程式可知反应物的分子中一共有2个碳原子、8个氢原子、6个氮原子和8个氧原子,生成物分子中有2个碳原子、6个氮原子、4个氧原子和4个X分子,根据质量守恒定律反应前后原子的种类和数目保持不变可知4个X分子中应该含有8个氢原子和4个氧原子,则X的化学式为![]() 。
。
(2)嫦娥四号使用了大量铝合金,铝不仅密度小,耐腐蚀能力也较强,铝的耐腐蚀能力较强的原因是铝与氧气反应在铝的表面形成一层致密的氧化物薄膜。
(3)由题意国旗的材料是用聚酰亚胺制成的,聚酰亚胺不是天然生成的,不属于天然高分子材料,金属材料包括纯金属与合金,聚酰亚胺也不是金属材料,聚酰亚胺属于合成高分子材料。
(4)根据镓元素在周期表中信息图及原子结构示意图可知:
A、镓元素的原子序数为31,镓原子核电荷数=核内质子数=核外电子数=原子序数=31,原子核由质子和中子构成,没有电子,A选项说法不正确,不符合题意;
B、镓的相对原子质量为69.72,相对原子质量的单位为“1”,通常省略不写,“g”是质量的单位,B选项说法不正确,不符合题意;
C、在原子结构示意图中核电荷数=核外电子数,则有![]() ,C选项说法正确,符合题意;
,C选项说法正确,符合题意;
D、一般情况下,最外层电子数小于4的,反应中容易失去电子形成稳定结构,大于4的反应中容易得到电子形成8电子的稳定结构,镓原子最外层电子数为3,在化学反应中易失去3个电子,D选项说法不正确,不符合题意。故选C。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:初中化学 来源: 题型:
【题目】某同学为探究碱的性质,对氢氧化钙进行如下实验。
(1)将石蕊试液滴入澄清石灰水中,振荡,溶液呈____色。
(2)将稀盐酸逐滴加入含有酚酞试液的石灰水中,振荡,可观察到什么现象?____
(3)将CO2气体通入澄清石灰水中,澄清石灰水变浑浊,说明氢氧化钙能与某些___(填物质类别)反应,氢氧化钙与氢氧化钠的化学性质相似,试写出三氧化硫与氢氧化钠反应的化学方程式___。
(4)向氢氧化钙和稀盐酸反应后的溶液中逐滴滴加Na2CO3溶液,溶液pH的变化如图所示,e点溶液中溶质的化学式是___,滴入Na2CO3溶液的过程中d~m段观察到的现象是____,m~n段观察到的现象是___。
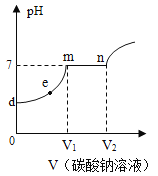
(5)称取5g含有氯化钠杂质的氢氧化钠样品,加入25g水后充分溶解,缓慢加入10%的稀盐酸,当溶液的pH=7时,刚好用去稀盐酸的量为36.5g。计算样品中氢氧化钠的质量分数____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)小明要用100g质量分数为10%的氢氧化钠溶液来制作“叶脉书签”,如图是他配制氢氧化钠溶液的实验操作示意图.
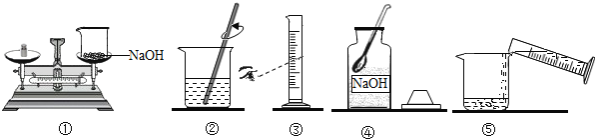
①量取所需要的水应选择_______(选填“10mL”、“50mL”或“100mL”)量筒.
②指出图中的2处操作错误,请写出其中的一处错误:________.
③用上述图示的序号表示配制溶液的操作顺序:_________.
④配置100g质量分数为10%的氢氧化钠溶液,需要氢氧化钠_______g.如果按图中③量取水的质量______(填“偏小”或“偏大”或“不变”)
(2)现用质量分数为12%的氢氧化钠溶液(密度约为1.09g/cm3)配置20g质量分数为6%的氢氧化钠溶液,需要质量分数为12%的氢氧化钠溶液________mL(计算结果精确到0.1),需要水_______mL(水的密度为1g/cm3)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下:

部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(1)熟石灰主要成分的化学式是____________。
(2)溶液A中的阳离子是___________________(填离子符号)。
(3)沉淀C的成分是_____________________。
(4)溶液B与熟石灰反应的化学方程式是____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属、酸、碱、盐在初中化学的学习中,是很重要的内容。
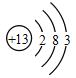
(1)如图为某元素的原子结构示意图,请写出由该元素组成的单质,常温下在空气中发生的变化的化学方程式_____。
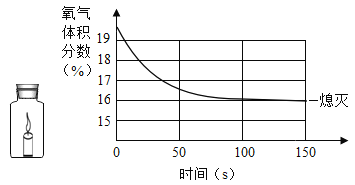
(2)实验小组成员将足量的蜡烛点燃,迅速放入集气瓶内,并将集气瓶密封。仪器测出集气瓶内的氧气含量变化如图所示。请你根据图示,写出实验数据呈现的一项结论_____。
(3)向100g含AgNO3、Cu(NO3)2和Fe(NO3)2的混合溶液中加入适量的Zn,充分反应后,Zn固体全部消失,过滤,得到滤液与滤渣,称得滤液的质量为100 g。
①请写出该反应中可能发生反应的化学方程式_____;
②请分析滤液质量与原混合溶液质量相等的原因_____。
(4)下图是制备气体的部分发生装置和收集装置。
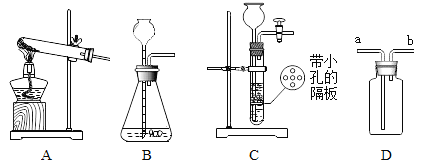
①若要选用高锰酸钾制取氧气,该反应的化学方程式为_____;
②图中的发生装置中,既可以用于实验室制取氧气、氢气,又可以用于实验室制取二氧化碳的发生装置为_;若制取的气体用D收集时从a进入,则制取该气体的化学方程式可能为_;
(5)钠着火不可以用二氧化碳来灭火,钠在二氧化碳中燃烧生成碳酸钠和炭黑。假若有9.2 g的金属钠在二氧化碳中完全燃烧,可生成炭黑的质量是多少_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回收利用是保护金属资源的一条有效途径。 某工业废料含氧化铜,氧化铁和不溶于酸的杂质,经过处理后可得到铜和硫酸亚铁溶液[![]() ]
]
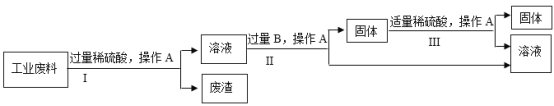
(1)步骤Ⅰ、Ⅱ、III都需进行操作A,操作A的名称为_______________。
(2)步骤Ⅰ中为加快反应速率,可采取的一种措施是_______________。
(3)步骤Ⅱ中除溶液颜色变化外,还可观察到_____________,判断加入B是否过量的方法是_______________。
(4)步骤III中发生反应的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为阻止“新型冠状病毒肺炎”的扩散,可使用过氧乙酸(化学式CH3COOOH)对公共场所、医疗器械及传染病房进行杀菌消毒。下列关于过氧乙酸的叙述正确的是( )
A.过氧乙酸的相对分子质量为76g
B.过氧乙酸中氧元素的质量分数为33.3%
C.过氧乙酸中碳、氢、氧元素质量比为6:1:12
D.过氧乙酸是由碳原子、氧原子和氢原子构成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铁矿的主要成分是二硫化亚铁(FeS2),其中硫元素的化合价为-1.由黄铁矿为原料生产硫酸的工业流程如下图所示。
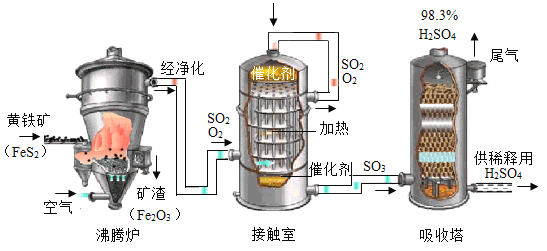
(1)生产的第一步将黄铁矿粉碎的目的是_____;
(2)生产的第二步是在接触室内将SO2转化成SO3,反应的化学方程式为_____;
(3)在生产过程中,化合价发生改变的元素有_____种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】银器发暗是因为形成了黑色的Ag2S。欲使银器变亮,可先用洗衣粉洗去表面油污,再把它和铝片放入碳酸钠溶液中共煮,至银器恢复银白色时,取出银器,用水洗净即可。发生反应的化学方程式为:2Al+3Ag2S+6H2O![]() 6Ag+2Al(OH)3+3X↑,X的化学式是
6Ag+2Al(OH)3+3X↑,X的化学式是
A. H2SB. SO2C. SO3D. O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com