
【题目】实验中,小红误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现也有气泡产生。为了解该气体的成分,实验小组进行了以下探究活动:
(提出猜想)小红猜想是氧气;小敏猜想是氢气;小雨猜想是二氧化碳。其他同学认为小雨的猜想是错误的,无需实验验证。理由是______;
(进行实验)利用图I所示的装置分别进行实验:

(1)小红:反应一段时间后,将带火星的木条放在a处,观察到______,则她的猜想错误。
(2)小敏:①用图II所示装置干燥从a导管出来的气体,将管口a与______(填“b”或“c“)端管口连接。
②反应一段时间,点燃干燥的气体,通过对现象的分析,得出他的猜想正确。
(得出结论)铝、氢氧化钠和水反应生成氢气和偏铝酸钠(NaAlO2),反应的化学方程式为______。
(交流讨论)有同学认为,小敏的实验步骤②中存在安全隐患,理由是______
(拓展提升)Ⅰ.某化学小组在AgNO3和Cu(NO3)2的混合溶液中加入一定质量的锌粉,充分反应后过滤,得到滤液和滤渣。他们对所得滤液和滤渣有如下描述:
①滤液中一定含有Zn(NO3)2 ;②滤渣中一定含有Ag,可能含有Cu和Zn;③若滤液呈蓝色,则向滤渣中滴加稀盐酸无明显现象;④若向滤渣中滴加稀盐酸有气泡产生,
则滤液中一定没有AgNO3和Cu(NO3)2。上述四种描述中正确的个数为(______)
A4个 B3个 C2个 D1个
Ⅱ.为测定镁和硫酸镁固体混合物中镁元素的质量分数,先称取混合物10g,放入一干净的烧杯中,然后取一定溶质质量分数的稀硫酸100g,平均分五次加入其中,充分振荡,实验所得数据如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 0.12 | x | 0.36 | 0.4 | y |
(l)上表中x=______、y=______.
(2)所用稀硫酸的溶质质量分数为______.(计算结果精确到0.1%)
(3)固体混合物中镁元素的质量分数为________?(第(3)题写出计算过程,计算结果精确到0.1%)
【答案】根据质量守恒定律,反应物中无碳元素,生成物不可能有二氧化碳 木条不复燃 c ![]() 氢气为可燃性气体,点燃之前应该验纯,否则有爆炸的危险 A 0.24 0.4 29.4% 设固体混合物中镁元素的质量为y,则有:
氢气为可燃性气体,点燃之前应该验纯,否则有爆炸的危险 A 0.24 0.4 29.4% 设固体混合物中镁元素的质量为y,则有:

由![]() 解得y=4.8g
解得y=4.8g
则固体混合物中硫酸镁的质量为10g-4.8g=5.2g;
则固体混合物中镁元素的质量为![]()
则固体混合物中镁元素的质量分数为![]()
答:固体混合物中镁元素的质量分数为58.4%。
【解析】
探究氢氧化钠溶液与金属铝反应产生的气泡的成分:
提出猜想:小红猜想是氧气;小敏猜想是氢气;小雨猜想是二氧化碳。其他同学认为小雨的猜想是错误的,无需实验验证。理由是根据质量守恒定律,反应物中无碳元素,生成物不可能有二氧化碳;
进行实验:
(1)小红:反应一段时间后,将带火星的木条放在a处,观察到木条不复燃,则她的猜想,该气体是氧气错误。
(2)小敏:①用图II所示装置干燥从a导管出来的气体,气体应该长导管进,短导管出,故将管口a与c端管口连接。
②反应一段时间,点燃干燥的气体,通过对现象的分析,得出他的猜想正确。
得出结论:铝、氢氧化钠和水反应生成氢气和偏铝酸钠(NaAlO2),反应的化学方程式为![]() 。
。
交流讨论:有同学认为,小敏的实验步骤②中存在安全隐患,理由是氢气为可燃性气体,点燃之前应该验纯,否则有爆炸的危险。
拓展提升:
Ⅰ、在AgNO3和Cu(NO3)2的混合溶液中加入一定质量的锌粉,充分反应后过滤,得到滤液和滤渣。锌会先与AgNO3发生置换反应,生成硝酸锌和银,若锌过量,反应完之后继续与Cu(NO3)2反应生成铜和硝酸锌,则有:
①滤液中一定含有Zn(NO3)2 ,说法正确;
②滤渣中一定含有Ag,若锌过量,可能含有Cu和Zn,说法正确;
③若滤液呈蓝色,说明溶液中有铜离子,锌的量不足,滤渣中没有锌,有银,可能有铜,则向滤渣中滴加稀盐酸无明显现象,说法正确;
④若向滤渣中滴加稀盐酸有气泡产生,说明滤渣中有锌,则原溶液中的AgNO3和Cu(NO3)2完全反应,则滤液中一定没有AgNO3和Cu(NO3)2,说法正确;
综上所述上述四种描述中正确的个数为4个, A选项正确,符合题意。故选A。
Ⅱ、根据题意和表格中的数据可知,第1次、第2次、第3次气体质量等比例增加,第3次到第4次没有成比例,则第4次加入后完全反应,第5次加入后不再产生气体,与第4次的质量相同,则有:
(l)表中x=0.24、y=0.4;
(2)由题意可知第1次加入20g稀硫酸产生0.12g氢气,设20g稀硫酸中溶质硫酸的质量为x,则有:

由![]() 解得x=5.88g
解得x=5.88g
则所用稀硫酸的溶质质量分数为![]()
答:所用稀硫酸的溶质质量分数为29.4%。
(3)设固体混合物中镁元素的质量为y,则有:

由![]() 解得y=4.8g
解得y=4.8g
则固体混合物中硫酸镁的质量为10g-4.8g=5.2g;
则固体混合物中镁元素的质量为![]()
则固体混合物中镁元素的质量分数为![]()
答:固体混合物中镁元素的质量分数为58.4%。


科目:初中化学 来源: 题型:
【题目】2019年是元素周期律发现150周年。如图是氯元素在元素周期表中的相关信息,下列说法错误的是( )
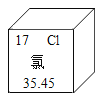
A. 氯属于金属元素
B. 氯的原子序数是17
C. 氯原子核外有17个电子
D. 氯的相对原子质量是35.45
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甘草磷是一种有机磷除草剂,白色晶体,易溶于水、乙醇等,其化学式为C3H8NO5P.计算:
(1)草甘膦的相对分子质量为_____
(2)草甘膦中碳元素、氢元素、氮元素的质量比为____(最简整数比)
(3)16.9克草甘膦中含有_______克膦元素
(4)_____克NH4NO3和338g草甘膦含氮量相等?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂排放的工业废水中含有硫酸亚铁和少量硫酸铜。下图是从该废水中回收金属铜和硫酸亚铁晶体的主要流程,请回答下列问题:
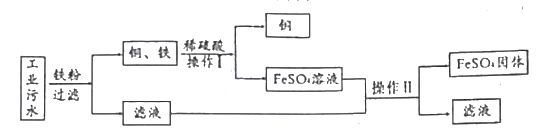
(1)工业废水中加入铁粉后发生反应的化学方程式为________。
(2)操作I名称为_______;玻璃棒在该操作中的用途为________。
(3)进行操作I前加入稀硫酸的目的是__________ ,能否用稀盐酸代替?(填“能”或“不能”),原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】大蒜素的化学式为C6H10S3,下列说法正确的是
A.大蒜素属于氧化物
B.大蒜素中硫元素的质量分数最低
C.大蒜素由6个碳原子、10个氢原子和3个硫原子构成
D.大蒜素中碳元素、氢元素和硫元素的质量比为36:5:48
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)将浑浊的河水用图1所示的简易净水器进行净化,其中活性炭的主要作用是_____,净化后得到的水属于_______(填“纯净物”或“混合物”)。
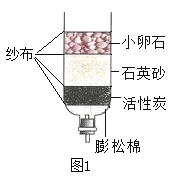
(2)生活中常用_____来区分硬水和软水,生活中降低水的硬度的方法是_______。
(3)下图是电解水的装置。
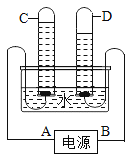
①试管D中收集的气体是_____,A是电源的_____极。
②理论上生成气体的体积比V(C)∶V(D)=________。
③原子是化学变化中的最小微粒,若a→c→b可表示一种化合反应,那表示分解反应的顺序应该是____。
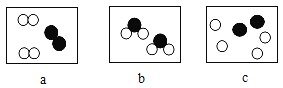
④运用分与合的思想都能证明水是___组成的化合物,请写出电解水的化学方程式___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒在人体中是非常少的微量元素,也是必不可少的微量元素。硒元素在周期表中的信息如图所示。下列说法不正确的是
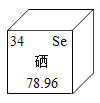
A.硒是非金属元素B.硒原子的核电荷数为34
C.硒的元素符号为SeD.硒元素的相对原子质量为78.96g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们从一水沟中取了一些浊水,请你参与他们的实验,并完成相关问题。
(1)向这些浊水中加入净水剂,并用玻璃棒搅拌,使水中悬浮的颗粒沉降下来。下列物质可作净水剂的是_____(填序号)。
A.食盐 B.高锰酸钾 C.明矾 D.肥皂水
(2)按如图甲所示的方法操作。仪器A的作用_____,实验中发现仪器 D 中的液体呈浑浊,你猜想其中的原因可能是_____(填一种)。
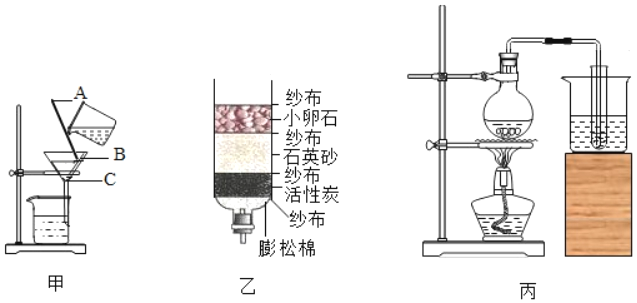
(3)改正之后获得一杯澄清的水。关于这杯水,下列描述一定正确的是_____
A.是氧化物 B.是硬水 C.是软水 D.是混合物
(4)如果这杯澄清的水有点颜色,使用如图乙所示的净水装置,能除去水的颜色的物质主要是_____主要是利用它的_____性。
(5)取少量经过净水器出来的水,向其中加入一些肥皂水,振荡,发现几乎没有泡沫,有大量的浮渣。据此现象你能得到的结论是_____
(6)用如图丙所示装置对经净水器出来的水进行处理。实验时圆底烧瓶中加入了几片碎瓷片,其作用是_____。烧杯中应该装_____(填“热水”或“冷水”),其作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于催化剂的叙述正确的是( )
A.催化剂在催化过程中所有的性质不变
B.同一个反应可以选用不同的催化剂
C.加入二氧化锰可以使过氧化氢产生更多的氧气
D.能加快物质的化学反应速率的是催化剂,减慢化学反应速率的不是催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com