
分析 (1)根据图2分析;
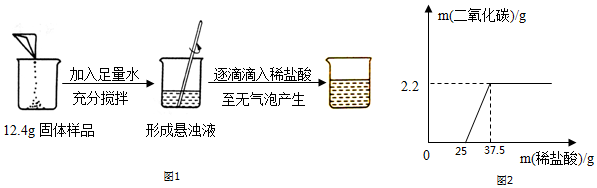
(2)根据图中信息分析可知,加入稀盐酸的质量为25g时开始反应产生CO2,至37.5g后不再有气体产生,总共产生2.2gCO2气体根据二氧化碳的质量计算碳酸钙的质量,进一步计算样品中氢氧化钙的质量分数.
(3)根据质量守恒定律分析.
解答 解:(1)由图2可知反应结束后产生二氧化碳的质量为2.2g;
(2)根据图中信息分析可知,加入稀盐酸的质量为25g时开始反应产生CO2,至37.5g后不再有气体产生,总共产生2.2gCO2气体.
设该样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
该样品中氢氧化钙的质量分数为$\frac{12.4g-5g}{12.4g}×100%$=59.7%.
答:该样品中氢氧化钙的质量分数为59.7%.
(3)根据质量守恒定律,反应前后元素的质量不变,碳酸钙中的钙元素转化为氯化钙中的钙元素,烧杯中钙元素的质量不变.
故答案为:(1)2.2;
(2)59.7%.
(3)不变.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题意(或图表信息)等各种信息,根据质量守恒定律计算出二氧化碳气体的质量是正确解答本题的前提和关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀盐酸、一定有气泡产生 | |
| D. | 反应后的滤液中溶质可能是一种或两种 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
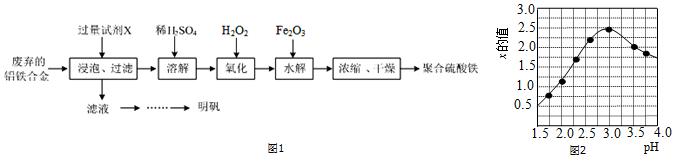
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe(NO3)2 | B. | Fe(NO3)3 | ||
| C. | Cu(NO3)2、Fe(NO3)2 | D. | AgNO3、Cu(NO3)2、Fe(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
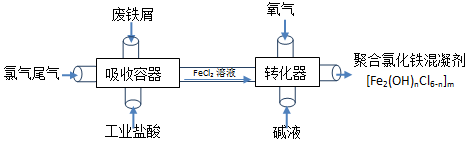
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | N2 | O2 | 将气体缓缓通过足量的灼热焦炭 |
| B | CaO | CaCO3 | 加水溶解、过滤 |
| C | Fe | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
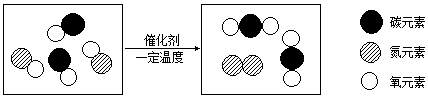
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com