
 ΈΣ≤βΕ®Ρ≥≥ύΧζΩσ ·÷–―θΜ·ΧζΒΡ÷ ΝΩΖ÷ ΐΘ§–ΓΝζΚΆΥϊΒΡΆ§―ß”ΟΉψΝΩΒΡ“Μ―θΜ·ΧΦ”κ10g≥ύΧζΩσ ·―υΤΖ≥δΖ÷Ζ¥”ΠΘ®‘”÷ ≤Μ≤Έ”κΖ¥”ΠΘ©Θ§≤ΔΫΪ…ζ≥…ΒΡΤχΧε”Ο“ΜΕ®ΝΩΒΡ«β―θΜ·ΡΤ»ή“ΚΆξ»ΪΈϋ ’Θ§ΗΟ»ή“ΚΉή÷ ΝΩ”κΖ¥”Π ±ΦδΒΡ±δΜ·ΙΊœΒ»γΆΦΘ°
ΈΣ≤βΕ®Ρ≥≥ύΧζΩσ ·÷–―θΜ·ΧζΒΡ÷ ΝΩΖ÷ ΐΘ§–ΓΝζΚΆΥϊΒΡΆ§―ß”ΟΉψΝΩΒΡ“Μ―θΜ·ΧΦ”κ10g≥ύΧζΩσ ·―υΤΖ≥δΖ÷Ζ¥”ΠΘ®‘”÷ ≤Μ≤Έ”κΖ¥”ΠΘ©Θ§≤ΔΫΪ…ζ≥…ΒΡΤχΧε”Ο“ΜΕ®ΝΩΒΡ«β―θΜ·ΡΤ»ή“ΚΆξ»ΪΈϋ ’Θ§ΗΟ»ή“ΚΉή÷ ΝΩ”κΖ¥”Π ±ΦδΒΡ±δΜ·ΙΊœΒ»γΆΦΘ°Ζ÷Έω ―θΜ·ΧζΚΆ“Μ―θΜ·ΧΦ‘ΎΗΏΈ¬ΧθΦΰœ¬Ζ¥”Π…ζ≥…ΧζΚΆΕΰ―θΜ·ΧΦΘ§Εΰ―θΜ·ΧΦΚΆ«β―θΜ·ΡΤΖ¥”Π…ζ≥…ΧΦΥαΡΤΚΆΥ°Θ§«β―θΜ·ΡΤ»ή“Κ‘ωΦ”ΒΡ÷ ΝΩΦ¥ΈΣΖ¥”Π…ζ≥…Εΰ―θΜ·ΧΦΒΡ÷ ΝΩΘ§ΗυΨίΕΰ―θΜ·ΧΦΒΡ÷ ΝΩΩ…“‘ΦΤΥψ―θΜ·ΧζΒΡ÷ ΝΩΘ§¥”ΕχΩ…“‘ΦΤΥψΗΟ≥ύΧζΩσ ·÷–Χζ‘ΣΥΊΒΡ÷ ΝΩΖ÷ ΐΘΜ
ΗυΨίΕΰ―θΜ·ΧΦΒΡ÷ ΝΩΩ…“‘ΦΤΥψ«β―θΜ·ΡΤΒΡ÷ ΝΩΘ§Ϋχ“Μ≤ΫΩ…“‘ΦΤΥψΥυ”Ο«β―θΜ·ΡΤ»ή“ΚΒΡ»ή÷ ÷ ΝΩΖ÷ ΐΘ°
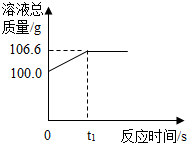
Ϋβ¥π ΫβΘΚΘ®1Θ©”…ΆΦ÷– ΐΨίΩ…÷ΣΘ§…ζ≥…Εΰ―θΜ·ΧΦΒΡ÷ ΝΩΈΣΘΚ106.6g-100.0g=6.6gΘ§
Ι ΧνΘΚ6.6Θ°
Θ®2Θ©…η―θΜ·ΧζΒΡ÷ ΝΩΈΣxΘ§
Fe2O3+3CO$\frac{\underline{\;ΗΏΈ¬\;}}{\;}$2Fe+3CO2Θ§
160 132
x 6.6g
$\frac{160}{x}$=$\frac{132}{6.6g}$Θ§
x=8gȧ
ΗΟ≥ύΧζΩσ ·÷–Χζ‘ΣΥΊΒΡ÷ ΝΩΖ÷ ΐΈΣΘΚ$\frac{8g}{10g}$ΓΝ100%=80%Θ§
Ι ΧνΘΚ80%Θ°
Θ®3Θ©…η«β―θΜ·ΡΤ÷ ΝΩΈΣyΘ§
2NaOH+CO2®TNa2CO3+H2OΘ§
80 44
y 6.6g
$\frac{80}{y}$=$\frac{44}{6.6g}$Θ§
y=12gȧ
Υυ”Ο«β―θΜ·ΡΤ»ή“ΚΒΡ»ή÷ ÷ ΝΩΖ÷ ΐΈΣΘΚ$\frac{12g}{100.0g}$ΓΝ100%=12%Θ§
¥πΘΚΥυ”Ο«β―θΜ·ΡΤ»ή“ΚΒΡ»ή÷ ÷ ΝΩΖ÷ ΐΈΣ12%Θ°
ΒψΤά Εΰ―θΜ·ΧΦΚΆ«β―θΜ·ΡΤ«ΓΚΟΆξ»ΪΖ¥”Π ±Θ§œϊΚΡ«β―θΜ·ΡΤ»ή“ΚΒΡ÷ ΝΩ «100.0gΘ§“ΣΉΔ“βάμΫβΘ°


 νΦΌœΈΫ”ΫΧ≤ΡΤΎΡ© νΦΌ‘ΛœΑΈδΚΚ≥ωΑφ…γœΒΝ–¥πΑΗ
νΦΌœΈΫ”ΫΧ≤ΡΤΎΡ© νΦΌ‘ΛœΑΈδΚΚ≥ωΑφ…γœΒΝ–¥πΑΗ ΦΌΤΎΉς“Β νΦΌ≥…≥Λά÷‘Α–¬Ϋ°«ύ…ΌΡξ≥ωΑφ…γœΒΝ–¥πΑΗ
ΦΌΤΎΉς“Β νΦΌ≥…≥Λά÷‘Α–¬Ϋ°«ύ…ΌΡξ≥ωΑφ…γœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΧνΩ’Χβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | 50% | BΘ° | 80% | CΘ° | 12.5% | DΘ° | 20% |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΧνΩ’Χβ
 œ÷≥Τ»ΓΧΦΥαΡΤ―υΤΖ6gΘ§≈δ÷Τ≥…»ή“ΚΘ§‘ΌœρΤδ÷–Φ”»κCaCl2»ή“ΚΘ§Ζ¥”Π ±CaCl2»ή“Κ”κ≥ΝΒμΒΡ÷ ΝΩΙΊœΒ»γΆΦΥυ ΨΘ°«κΫβΨω“‘œ¬Έ ΧβΘΚ
œ÷≥Τ»ΓΧΦΥαΡΤ―υΤΖ6gΘ§≈δ÷Τ≥…»ή“ΚΘ§‘ΌœρΤδ÷–Φ”»κCaCl2»ή“ΚΘ§Ζ¥”Π ±CaCl2»ή“Κ”κ≥ΝΒμΒΡ÷ ΝΩΙΊœΒ»γΆΦΥυ ΨΘ°«κΫβΨω“‘œ¬Έ ΧβΘΚ≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
 Ρ≥―–ΨΩ–‘―ßœΑ–ΓΉι‘Ύ–≠÷ζάœ Π«εάμ Β―ι “ ±Θ§ΖΔœ÷“Μ≈ζ¥φΖ≈ΕύΡξΒΡ«β―θΜ·ΗΤΘ°ΈΣΦλ―ιΤδ±δ÷ «ιΩωΘ§Ϋχ––ΝΥ»γœ¬ΧΫΨΩΘΚ»Γ«β―θΜ·ΗΤ―υΤΖ11.4g”ΎΉΕ–ΈΤΩ÷–Θ§Φ”»κ38.6gΥ°Θ§’ώΒ¥–Έ≥…–ϋΉ«“ΚΘ§Ζ≈‘ΎΒγΉ”ΧλΤΫ…œΘ§œρΉΕ–ΈΤΩ÷–÷πΒΈΒΈΦ”14.6%ΒΡœΓ―ΈΥαΘ§»γΆΦΦΉΥυ ΨΘ§’ώΒ¥ΚσΕΝ»Γ÷ ΝΩΘ°ΒΟΒΫΉΕ–ΈΤΩ÷–Έο÷ ΒΡ÷ ΝΩ”κœΓ―ΈΥα÷ ΝΩΙΊœΒΘ§»γΆΦ““Υυ ΨΘ§ ‘«σΘΚ
Ρ≥―–ΨΩ–‘―ßœΑ–ΓΉι‘Ύ–≠÷ζάœ Π«εάμ Β―ι “ ±Θ§ΖΔœ÷“Μ≈ζ¥φΖ≈ΕύΡξΒΡ«β―θΜ·ΗΤΘ°ΈΣΦλ―ιΤδ±δ÷ «ιΩωΘ§Ϋχ––ΝΥ»γœ¬ΧΫΨΩΘΚ»Γ«β―θΜ·ΗΤ―υΤΖ11.4g”ΎΉΕ–ΈΤΩ÷–Θ§Φ”»κ38.6gΥ°Θ§’ώΒ¥–Έ≥…–ϋΉ«“ΚΘ§Ζ≈‘ΎΒγΉ”ΧλΤΫ…œΘ§œρΉΕ–ΈΤΩ÷–÷πΒΈΒΈΦ”14.6%ΒΡœΓ―ΈΥαΘ§»γΆΦΦΉΥυ ΨΘ§’ώΒ¥ΚσΕΝ»Γ÷ ΝΩΘ°ΒΟΒΫΉΕ–ΈΤΩ÷–Έο÷ ΒΡ÷ ΝΩ”κœΓ―ΈΥα÷ ΝΩΙΊœΒΘ§»γΆΦ““Υυ ΨΘ§ ‘«σΘΚ≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| ―Γœν | Έο÷ Θ®‘”÷ Θ© | ≤ΌΉςΖΫΖ® |
| A | CO2Θ®H2OΘ© | ΫΪΤχΧεΆ®Ιΐ Δ”–ΜπΦνΒΡΗ…‘οΙή |
| B | CuΘ®CuOΘ© | Ά®»κΉψΝΩ―θΤχ≤ΔΦ”»» |
| C | CO2Θ®COΘ© | Βψ»Φ |
| D | FeCl2Θ®CuCl2Θ© | Φ”»κΉψΝΩΧζ–ΦΘ§≥δΖ÷Ζ¥”ΠΚσΙΐ¬Υ |
| AΘ° | A | BΘ° | B | CΘ° | C | DΘ° | D |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | NaOHΓΔNa2SO4ΓΔNaCl | BΘ° | NaClΓΔNaOHΓΔNa2SO4 | ||
| CΘ° | NaClΓΔNa2SO4ΓΔNaOH | DΘ° | Na2SO4ΓΔNaClΓΔNaOH |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ≥θ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com