
 在50g7.3%的盐酸中逐滴加入一定溶质质量分数的氢氧化钠溶液,得到如图所示的图象,求所加氢氧化钠溶液的溶质的质量分数.
在50g7.3%的盐酸中逐滴加入一定溶质质量分数的氢氧化钠溶液,得到如图所示的图象,求所加氢氧化钠溶液的溶质的质量分数. 分析 稀盐酸与氢氧化钠溶液反应生成氯化钠和水,由图示可知,恰好完全反应时消耗的氢氧化钠溶液的质量为40g;由参加反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式列式计算出所加氢氧化钠溶液的溶质的质量分数.
解答 解:50g7.3%的盐酸中含溶质的质量为50g×7.3%=3.65g.
设参加反应的稀盐酸的质量为x
HCl+NaOH═NaCl+H2O
36.5 40
3.65g x
$\frac{36.5}{40}=\frac{3.65g}{x}$ x=4g
所加氢氧化钠溶液的溶质的质量分数为$\frac{4g}{40g}×$100%=10%.
答:所加氢氧化钠溶液的溶质的质量分数为10%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.


科目:初中化学 来源: 题型:解答题
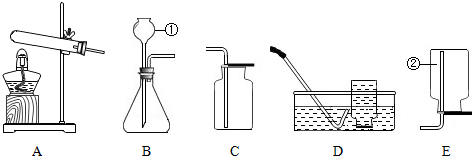
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
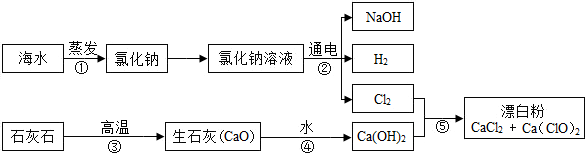
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 凡是溶液,其中溶剂的量一定大于溶质的量 | |
| B. | 凡是无色透明的液体都是溶液 | |
| C. | 由一种或多种物质分散在一种液体里所形成的混合物就是溶液 | |
| D. | 只要温度不变,溶剂的量不减少,溶液中的溶质就不会沉降或出现分层现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
| ①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中. | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II. | 锈蚀的速率I<II;铁的锈蚀速率与反应时的温度有关,温度越高,铁的锈蚀速率越快. |
| ②氧气含量 | 在相同温度下,向I、II两套装置的集气瓶中分别通入氧气和空气. | 铁钉均锈蚀,且U型管中液面由b处上升至a处所需时间I<II. | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快. |
| ③水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇. | 两套装置中铁钉均锈蚀; 且U型管中液面均由b处上升至a处,则所需时间I<II. | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com