
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加足量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: |

| 106 |
| 44 |
| x |
| 2.2g |
| 5.3g |
| 6g |


科目:初中化学 来源: 题型:
| A、Pb3O4 |
| B、Pb3O5 |
| C、PbNO |
| D、Pb2O5 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
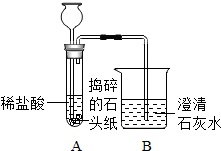 2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是碳酸钙.某化学兴趣小组的同学对“石头纸”的成分进行如右图所示的实验探究,观察到澄清石灰水变浑浊.请回答下列问题:
2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是碳酸钙.某化学兴趣小组的同学对“石头纸”的成分进行如右图所示的实验探究,观察到澄清石灰水变浑浊.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
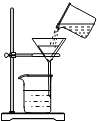 于博雅同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末,搅拌溶解,静置一会儿后,采用如图所示装置进行过滤.请问:
于博雅同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末,搅拌溶解,静置一会儿后,采用如图所示装置进行过滤.请问:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
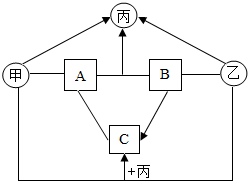 如图中A、B、C、甲、乙、丙均是初中化学常见的纯净物,其中甲、乙、丙为氧化物,A、B、C分别为含有三种元素的酸、碱、盐,且B、C中包含两种相同的元素.将B的饱和溶液升温有固体析出,且甲和丙反应能生成B.A的浓溶液在空气中放置一段时间后质量增加,其溶质中含氧元素约65.3%.图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在相应的转化关系,部分反应物、生成物及反应条件已略去.
如图中A、B、C、甲、乙、丙均是初中化学常见的纯净物,其中甲、乙、丙为氧化物,A、B、C分别为含有三种元素的酸、碱、盐,且B、C中包含两种相同的元素.将B的饱和溶液升温有固体析出,且甲和丙反应能生成B.A的浓溶液在空气中放置一段时间后质量增加,其溶质中含氧元素约65.3%.图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在相应的转化关系,部分反应物、生成物及反应条件已略去.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com