
| 药品 实验编号 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | m g,块状 | m g,块状 | m g,粉末状 | m g,粉末状 |
| 盐酸(过量) | w g,稀盐酸 | w g,浓盐酸 | w g,稀盐酸 | w g,浓盐酸 |
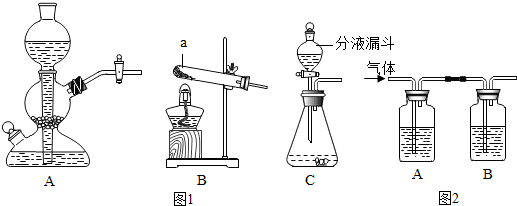
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C |
分析 ①搭建B装置时,酒精灯应在固定仪器a之前放置,以便于调节酒精灯火焰和试管底部的距离;
高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
②通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
③实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
进行对比试验要确定好常量和变量;
浓盐酸易挥发;
稀盐酸和氢氧化钙反应生成氯化钙和水,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水;
④块状大理石和稀盐酸接触面积不大,并且比较均匀;
分液漏斗能够控制液体样品的流量,从而可以控制反应速率.
解答 解:①搭建B装置时,酒精灯应在固定仪器a之前放置;
用此装置作为实验室高锰酸钾制氧气的发生装置,需要进行的改进是在试管口塞一团棉花.
故填:前;在试管口塞一团棉花.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③I.上述实验中反应的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
II.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照,这是因为乙中大理石的规格完全一致.
故填:乙.
III.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是反应物的接触面积.
故填:反应物的接触面积.
IV.实验室制取二氧化碳通常选择稀盐酸而不选择浓盐酸,理由是浓盐酸易挥发,导致二氧化碳中含有氯化氢;
图2的两个洗气瓶中都装有澄清石灰水,将使用浓盐酸制得的二氧化碳从左端通入时,稀盐酸和氢氧化钙反应生成氯化钙和水,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,观察到的现象是A中无明显现象,B中澄清石灰水变浑浊.
故填:浓盐酸易挥发,导致二氧化碳中含有氯化氢;A中无明显现象,B中澄清石灰水变浑浊.
Ⅴ.A、反应物接触面积更大,反应物浓度更大,因此反应更为剧烈;
B、由于浓盐酸易挥发出氯化氢气体,因此最终剩余溶液的质量更小;
C、产生的二氧化碳的质量相等;
D、大理石利用率相同.
故填:AB.
④实验如下表所示:
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | 反应物接触面积不大 |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C | 分液漏斗能够控制过氧化氢溶液的流量 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:选择题
| A. | 为了保护水资源,禁止使用化肥和农药 | |
| B. | 冰块与水混合得到纯净物 | |
| C. | 生活中可通过蒸馏降低水的硬度 | |
| D. | 河水经沉淀、过滤处理后得到纯水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 甲同学为了探究实验室中久置的NaOH的变质程度,他设计了如下的研究性学习课题报告,请你帮助加以完善.
甲同学为了探究实验室中久置的NaOH的变质程度,他设计了如下的研究性学习课题报告,请你帮助加以完善.| Na2CO3的质量 | |
| 变质NaOH的质量 | |
| NaOH的变质程度(用质量分数表示) |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 用高锰酸钾制氧气时,向高锰酸钾中加入少量MnO2--加快分解速度 | |
| B. | 滴瓶中胶头滴管滴完液体后,立即放回原瓶--防止药液被污染 | |
| C. | 盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞--防止溶液变质 | |
| D. | 实验室贮存白磷时,将其浸没在冷水中--防止发生自燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
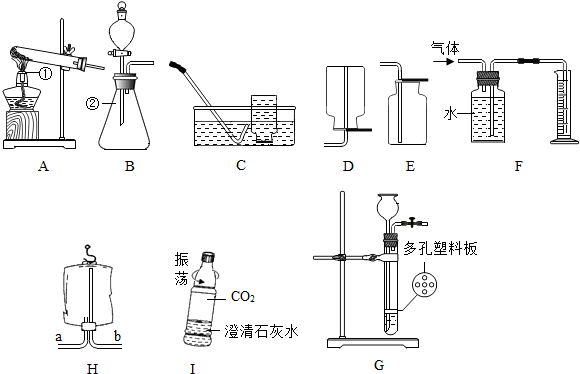
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| B. | 铁丝加入硫酸铜溶液有红色固体生成 | |
| C. | 电解水时正、负两极生成气体体积之比为2:1 | |
| D. | 木炭在氧气中燃烧发出白光 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
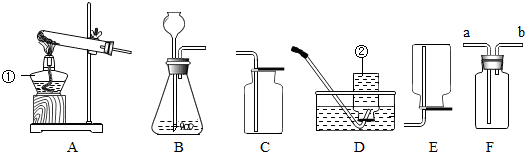
| 试管编号 | 1 | 2 | 3 | |
| 材料名称 | 无 | 苹果 | 土豆 | |
| 实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
| 产生气泡 | 很少 | 比1中多 | 较多 | |
| 复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
| 实验结论 | ||||
| 实验编号 | 1 | 2 | 3 |
| 过氧化氢溶液浓度 | 5% | 15% | 30% |
| 所用时间(秒) | 205 | 25 | 3 |
| 实验结论 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com