
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 | 溶液由红色变为无色且有气泡产生. | 小红 的猜想不正确 |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液. | 出现白色沉淀 | 小亮的猜想正确 |
| 3.继续向试管B中加入过量的稀盐酸 | 沉淀一部分消失,并生成气泡 |
分析 根据将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加几滴无色酚酞,溶液变为红色.说明没有氯化铜,溶液呈碱性;
说明杂质中含有碱性物质,碳酸钠和氢氧化钠溶液都显碱性,不能判定一定含有氢氧化钠和碳酸钠,只能确定含有其中的一种或都含有;硫酸钠溶液为中性,(不影响溶液的酸碱性)也不能判断是否含有;
解答 解:将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加几滴无色酚酞,溶液变为红色.说明没有氯化铜,溶液呈碱性;
说明杂质中含有碱性物质,碳酸钠和氢氧化钠溶液都显碱性,不能判定一定含有氢氧化钠和碳酸钠,只能确定含有其中的一种或都含有;硫酸钠溶液为中性,(不影响溶液的酸碱性)也不能判断是否含有;碳酸钠和硫酸反应生成二氧化碳、水和硫酸钠;氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠;
氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠;
【实验探究】
1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸,溶液由红色变为无色且有气泡产生.说明有氢氧化钠和碳酸钠,小红猜想不正确;
2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液.出现白色沉淀,而白色沉淀中加入稀盐酸,沉淀一部分消失,并生成气泡:再次说明,白色沉淀为碳酸钡或硫酸钡;因为碳酸钡与盐酸反应生成二氧化碳气体.而硫酸钡不与盐酸反应.
酚酞遇碱变红色,以及所加氯化钡是过量的,由于A溶液中有硫酸钠或者还有剩余的碳酸钠,由于最后实验加入了过量的盐酸,所以将试管A、B中的物质倒在同一烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质有HCl和 NaCl;
答案:
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 | 溶液由红色变为无色且有气泡产生. | 小红: 的猜想不正确 |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液. | 出现白色沉淀 | 小亮的猜想正确 |
| 3.继续向试管B中加入过量的稀盐酸 | 沉淀一部分消失,并生成气泡 |
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
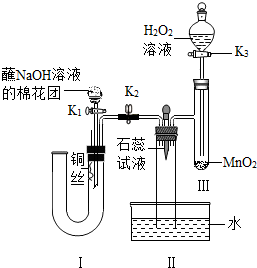 某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)
某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
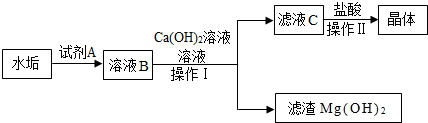
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH NaCl KNO3 MgCl2 | B. | NaOH Na2CO3 NaCl H2SO4 | ||
| C. | NaCl Na2SO4 AgNO3 HNO3 | D. | FeSO4 NaNO3 KCl HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
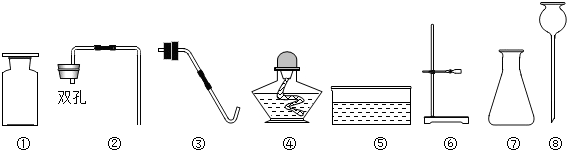
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可燃性气体点燃前一定要验纯 | |
| B. | 将煤制成蜂窝煤,能增大与空气的接触面积 | |
| C. | 堆放杂物的纸箱着火用水浇灭,降低了可燃物的着火点 | |
| D. | 食物的腐烂、动植物的呼吸都属于缓慢氧化 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
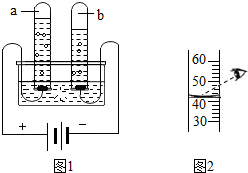
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com