
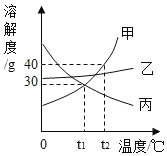
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲和丙的溶解度相等
B.降温可使丙物质的不饱和溶液变成饱和溶液
C.t1℃时,甲、乙和丙各 30g 分别加入 100g 水中,均形成饱和溶液
D.t2℃时,将 30g 甲物质加入 100g 水中,再降温到 t1℃时,所得溶液溶质的质量分数不变
【答案】D
【解析】
A、如图所示,t1℃时,甲和丙的溶解度曲线出现了交点,说明该温度时二者的溶解度相等,A选项说法不正确,不符合题意;
B、由丙的溶解度曲线可知丙的溶解度随着温度的升高而减小,升温可使丙物质的不饱和溶液变成饱和溶液,B选项说法不正确,不符合题意;
C、t1℃时,甲和丙的溶解度为30g,乙的溶解度大于30g,该温度下,甲、乙和丙各30g分别加入100g水中,甲和丙形成饱和溶液,乙形成的是不饱和溶液,C选项说法不正确,不符合题意;
D、甲的溶解度随着温度的升高而增大,t1℃时,甲的溶解度为30g,t2℃时,甲的溶解度为40g,t2℃时,将30g甲物质加入100g水中,得到不饱和溶液,降温到t1℃时,恰好为饱和溶液,没有溶质析出,所得溶液溶质的质量分数不变,D选项说法正确,符合题意。故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】查阅资料发现,氯化铵固体与亚硝酸钠固体混合加热也能制取氮气。反应的化学方程式如下:![]() 。利用此原理,静香同学想粗略测定某氯化铵样品中氯化铵的质量分数,设计了如下实验。(样品中的杂质不参与反应)实验步骤:(已知室温时,氮气的密度等于1.25g/L。)
。利用此原理,静香同学想粗略测定某氯化铵样品中氯化铵的质量分数,设计了如下实验。(样品中的杂质不参与反应)实验步骤:(已知室温时,氮气的密度等于1.25g/L。)
①按如图连接仪器,检查装置气密性。
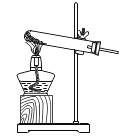
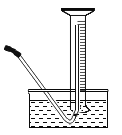
②将0.6g样品与足量NaNO2充分混合,并放入试管。在500mL规格的量筒内装满水后倒扣在水槽内。
③充分加热药品,并收集氮气。
④反应结束时,先熄灭酒精灯,并保持装置不动。
⑤等到实验仪器温度降至室温,将导管从量筒中取出。
⑥读取量筒内水的体积为276mL,进行计算。
(1)利用图示所用方法收集氮气,体现氮气具有______的性质。
(2)小夫同学认为静香同学的实验步骤设计存在问题,你支持谁的观点______。(若你支持小夫同学的观点请简要说明理由,若支持静香同学的观点不需再做其它说明。)
(3)试根据以上数据,计算该样品中氯化铵的质量分数______。(计算结果保留至小数点后1位)
(4)你认为以下操作可能导致测定的氯化铵质量分数偏小的是______(填写序号)
a.加热药品不充分 b.实验仪器没有冷却到室温 c.读数时俯视读数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na)。某品牌味精包装上标注内容如右图所示,请回答:

(1)谷氨酸钠分子中含有____种元素。
(2)谷氨酸钠的相对分子质量为 。
(3)谷氨酸钠中氢元素与氧元素的质量比为____。
(4)该味精每包含氯化钠的质量为 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将10g氯化钠、硫酸钠和硫酸钡的固体混合物放入烧杯中,加入100g水充分溶解,此时烧杯中未溶解的固体质量为2g,再向其中加入96.66g氯化钡溶液恰好完全反应,过滤后得到固体质量为6.66g。计算:
(1)原固体混合物中硫酸钠的质量。
(2)恰好完全反应时所得溶液的溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从ZnSO4、CuSO4和FeSO4的混合液中回收金属铜,设计了如下方案:
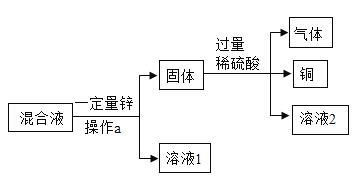
①操作a的名称是______,加入锌后,写出发生反应的一个化学方程式__,该反应体现了铜的金属活动性比锌____(选填“强”或“弱”)。
②操作a后的固体中一定有的物质是____,生成气体的化学式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质除杂是化学实验中经常遇到的问题。
实验一:为除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案。
实验方案 | |
方案 A |
|
方案 B |
|
方案 C |
|
上述方案中有两个方案是合理的,他们是___________写出合理方案中任意一个反应的化学方程式 ____________。
实验二:由于粗盐中含有少量 MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图:
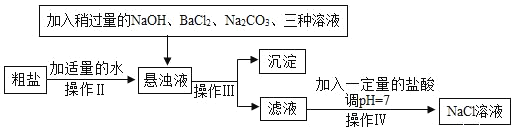
(1)加入稍过量的 Na2CO3溶液除了能除去粗盐中的 CaCl2外,它还有一个作用是 _____________(用化学方程式表示)
(2)实验操作Ⅲ是_____________,要用到的实验玻璃仪器是玻璃棒、漏斗和 ________________。
(3)如果稍过量的试剂加入的顺序依次为:Na2CO3、 NaOH、 BaCl2和盐酸,则最后得到的氯化钠溶液中一定含有杂质________________。
(4)操作Ⅳ的方法可以是:先在滤液中滴入酚酞溶液,再逐滴滴入盐酸直到滤液的 pH=7 的依据的现象是溶液由____________,如果加入的盐酸有点过量了,对后面 NaCl 溶液的结晶是否有影响______(是或否)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2020年3月22日是第二十八届“世界水日,3月22日8日是第三十三届“中国水周"。联合国确定2020年“世界水日”的主题为“Waterandclimatechange"(水与气候变化)我国纪念2020年“世界水日”和“中国水周”活动的主题为“坚持节水优先,建设幸福河湖”
(1)实验室电解水示意图如下:电解水反应装置,电解水的微粒运动过程
①图中“左”接低压直流电源的___极,a、b两支玻璃管中气体体积比约为___; 化学反应方程式为_____;

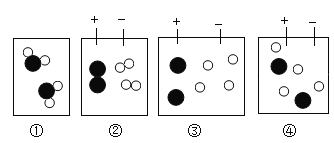
②图中能从微观角度合理表达水电解过程的数字编号顺序为_____;根据实验得出的结论是___。
③用溶质质量分数1%的氢氧化钠水溶液100g 进行电解,当溶液中氢氧化钠的溶质质量分数升高到2%时停止电解,理论上生成氢气质量为___。
(2)乐乐小组在一次游玩棋盘山时,用水瓶带回水库的水样准备净化的流程图如下

④水样中加入明矾的作用是___。
⑤操作A为___,用到的玻璃仪器有___。
⑥向液体 B中加活性炭,是利用其___的结构吸附水中的色素和异味。
⑦在整个实验净化流程中,能得到纯净水的操作是___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将20g碳酸钠和氯化钠固体混合物,加入101g水中完全溶解后,再往其中加入100g氯化钙溶液,恰好完全反应。过滤,将滤渣干燥,称得其质量为10g。试计算:
(1)反应后所得溶液的溶质质量分数。
(2)原固体混合物中所含钠元素的质量分数(计算结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用表中装置进行下列实验。已知:白磷的着火点为40℃。
实验装置 | 实验步骤 |
| Ⅰ.集气瓶的容积为250mL,实验开始前在集气瓶内加入50mL蒸馏水;在燃烧匙内加入足量白磷,塞紧瓶塞;取下注射器,吸入足量的、红颜色的水,再连接好装置。 Ⅱ.将组装好的实验装置转移到80℃热水中浸泡,片刻后白磷燃烧。 Ⅲ.待白磷熄灭后,再将整套装置放入冷水中冷却至室温。 |
(1)组装仪器后,用手向上拉动注射器活塞。松开手后,观察到________________,说明此装置气密性良好。
(2)冷却后进入集气瓶的红颜色的水的体积是_____mL。
(3)若在以上实验过程中,同时完成“验证可燃物燃烧需要满足温度达到着火点的条件”,还需补充的实验操作及现象是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com