
| A. | 碳酸、酒石酸都不是强酸 | |
| B. | 对人而言,酒石酸是必需的营养品 | |
| C. | MgCO3、NaHCO3与胃酸作用产生CO2,在服药后有喝汽水的舒服感 | |
| D. | 酒石酸钠水解显酸性 |
分析 根据一般可用含MgCO3或NaHCO3的药物治疗胃酸(盐酸)过多,利用酸与盐发生的化学反应来分析解答.
解答 解:A、酒石酸钠与盐酸反应会生成碳酸、酒石酸,两者都不是强酸,从而起到消耗胃酸的作用,此题考察强酸置换弱酸的知识,故A正确.
B、对人体而言酒石酸不是营养品,故B错误;
C、MgCO3、NaHCO3与胃酸作用产生CO2,但是为了治疗胃酸过多,而不是为了在服药后有喝汽水的舒服感,故C错误;
D、酒石酸是弱酸,故酒石酸钠水解呈碱性,故D错误.
故选A.
点评 本题考查胃酸的治疗,学生应从酸与盐反应的角度来认识治疗胃酸过多的原因,并学会将所学知识进行迁移应用来解释生活中常见的问题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
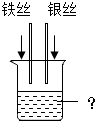 某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液.实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与.
某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液.实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
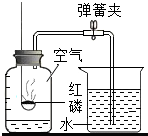 某同学用如图所示装置测定空气中氧气的体积分数,请你填写有关空格.
某同学用如图所示装置测定空气中氧气的体积分数,请你填写有关空格.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定存在Cl- | B. | 一定存在CO32-,可能存在Ba2+ | ||
| C. | 一定存在K+ | D. | 一定存在SO42-可能存在Ca2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
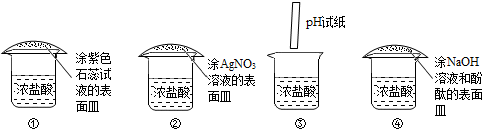
| A. | ② | B. | ②④ | C. | ④ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com