
| 实验 编号 | 温度(℃) | 大理石 规格 | 盐酸浓度(均取100mL) | 实验目的 |
| ① | 20 | 粗颗粒 | 20% | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和④探究温度对该反应速率的影响; (Ⅲ)实验①和③探究大理石规格(粗、细)对该反应速率的影响; |
| ② | 20 | 粗颗粒 | 10% | |
| ③ | 细颗粒 | 20% | ||
| ④ | 粗颗粒 |
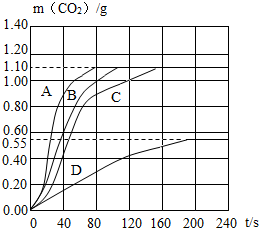
分析 根据实验的目的和影响化学反应速率的因素“浓度、温度、接触面积”来设计实验.
解答 解:(1)实验目的是探究浓度、温度、接触面积对反应速率的影响,故:
(Ⅰ)由于①和②探究浓度对反应速率的影响,故稀盐酸的浓度不同,应该是20%;
(Ⅱ)实验①和④探究温度对该反应速率的影响,故温度不同,应该选30℃,故答案为:④;
(Ⅲ)实验①和③的大理石规格不同,探究的是固体物质的表面积对反应速率的影响,故答案为:③;
故答案为:
| 实验 编号 | 温度(℃) | 大理石规格 | HCl浓度 | 实验目的 |
| ① | 20 | 粗颗粒 | 20% | (Ⅰ)实验①和②探究HCl浓度对该反应速率的影响; (Ⅱ)实验①和④探究温度对该反应速率的影响;(Ⅲ)实验①和③探究大理石规格 (粗、细)对该反应速率的影响 |
| ② | 20 | 粗颗粒 | 10% | |
| ③ | 20 | 细颗粒 | 20% | |
| ④ | 30 | 粗颗粒 | 20% |
点评 本题主要考查浓度、温度、接触面积对反应速率的影响,较好的考查了学生综合应用的能力


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:初中化学 来源: 题型:解答题
| 实验方案 | 实验现象 | 结论与解释 |
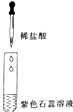 | 紫色石蕊试液变成红色 | 盐酸能与指示剂作用 |
 | 铁锈消失,溶液由无色变成黄色 | 盐酸能与金属氧化物反应,化学方程式为 Fe2O3+6HCl═2FeCl3+3H2O |
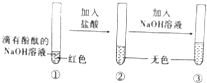
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含C |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
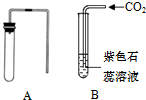 同学们在实验室用10%的稀盐酸和石灰石制取二氧化碳并进行二氧化碳性质实验.
同学们在实验室用10%的稀盐酸和石灰石制取二氧化碳并进行二氧化碳性质实验.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
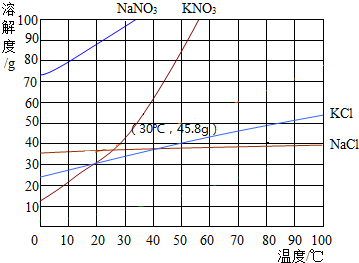 如图为几种固体的溶解度曲线,回答下列问题:
如图为几种固体的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
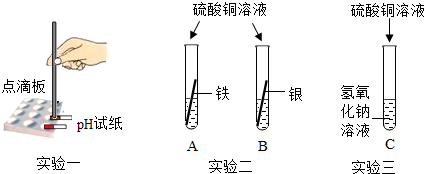
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com