【答案】
分析:(1)直接写出化学方程式
(2)与反应物的接触面积越大,反应速率越快
(3)加上灯罩可以使火焰更集中,提升温度
(4)装置改进:
将卧式改为直立式,同时用火焰把试管包住会影响,火焰与氧气的接触面积变小
实验研究:
通过实验可以看出氧化铜和碳粉的比例不同,得到产物也不同,从实验结果中可以得出该题答案,即反应最完全的.
反思交流:
在碳和氧化铜反应的过程中可能会产生一氧化碳气体,而一氧化碳有毒
提出问题:
题目中验证的是反应物的质量比例,对于反应的温度、反应的形状等都可能对反应速率有影响
解答:解:(1)直接写出化学方程式
(2)与反应物的接触面积越大,反应速率越快,所以把块状的木炭变成碳粉更利于反应的进行
(3)加上灯罩可以使火焰更集中,提升温度,利于反应的进行
(4)装置改进:将卧式改为直立式,同时用火焰把试管包住会影响,火焰与试管底部的接触面积变大,可以充分利用燃烧产生的热量;
实验研究:
通过实验可以看出氧化铜和碳粉的比例不同,得到产物也不同,从实验结果中可以得出该题答案,即反应最充分的.
反思交流:
在碳和氧化铜反应的过程中可能会产生一氧化碳气体,而一氧化碳有毒,会污染空气,所以要在最后设置一个尾气处理装置.
提出问题:
题目中验证的是反应物的质量比例,对于反应的温度、反应的形状等都可能对反应速率有影响
故答案为:
(1)直接写出化学方程式C+2CuO
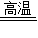
2Cu+CO
2↑
(2)增大反应物的接触面积,使反应更充分
(3)使火焰更集中
(4)装置改进:是;提高热效率,受热更均匀
实验研究:反应物的比例;1:10~1:11
反思交流:尾气没有处理,过程中可能产生的一氧化碳会污染环境;装石灰水的试管加上双孔橡皮塞,然后把尾气烧掉(或把排出一氧化碳的导管放在酒精喷灯下点燃或用气球收集起来.)
提出问题:反应物的形状(或反应温度)
点评:本题在考查“影响反应速率的因素”这个知识点时,采用了多个不同的例子,通过对比实验,得到结果分析生成结论,注重考查学生的分析问题和解决问题的能力.


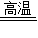 2Cu+CO2↑
2Cu+CO2↑



 (2011?闵行区一模)t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成下图中的斜线.下列说法正确的是( )
(2011?闵行区一模)t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成下图中的斜线.下列说法正确的是( )