
 胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g.某患者每日分泌盐酸溶质质量为8.5g,为治疗胃酸过多需服用如图所示的抑酸剂.
胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g.某患者每日分泌盐酸溶质质量为8.5g,为治疗胃酸过多需服用如图所示的抑酸剂.分析 服用抑酸剂是氢氧化镁和盐酸反应生成氯化镁和水,由于每天服用两次,每次服用两片,所以计算时要注意这些限制,根据对应化学方程式和氢氧化镁的质量计算消耗的HCl的质量,然后和分泌量对比.
解答 解:设每天消耗的HCl的质量为x
2HCl+Mg(OH)2=MgCl2+2H2O
73 58
x 0.29g×2×2
$\frac{73}{58}$=$\frac{x}{0.29g×2×2}$
x=1.46g
服用抑酸剂后剩余盐酸的质量为8.5g-1.46g=7.04g介于6.5g~7.3g之间,也就是恢复到正常范围了.
答:按照规定剂量服用后胃酸恢复到正常范围了.
点评 实际应用题,要在过程中转化为化学的问题,也就是提炼与化学内容直接相关的形式后分析解答和计算.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
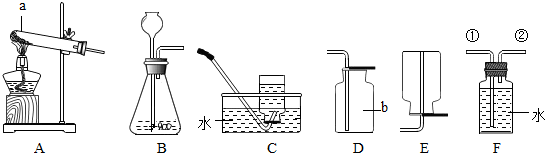
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | M可能是碳酸氢钠 | B. | M的化学性质很稳定 | ||
| C. | M中有氨气 | D. | M由四种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不能用铁器盛放硫酸铜溶液的原因:Fe+CuSO4═FeSO4+Cu 置换反应 | |
| B. | 铝耐腐蚀的原因:4Al+3O2═Al2O3 氧化反应 | |
| C. | 工业上以赤铁矿为原料冶炼生铁:2Fe2O3+3C $\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ 还原反应 | |
| D. | 电解水产生氢气和氧气:2H2O $\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ 分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com