
【题目】如图是两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图:
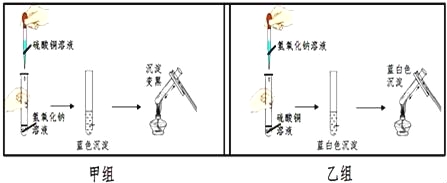
【甲组】氢氧化钠与硫酸铜反应的化学方程式为 ,加热后产生黑色的氧化铜。
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:
6NaOH+4CuSO4═3Na2SO4+Cu4(OH)6SO4↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因作出以下猜想:
猜想Ⅰ:硫酸铜溶液呈酸性; 猜想Ⅱ:生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH (填“>”、“<”或“﹦”),硫酸铜溶液呈酸性,猜想Ⅰ成立。
实验②:向盛有硫酸钠溶液的试管中逐滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈 (填“酸”、“中”或“碱”)性,猜想Ⅱ不成立。
【交流和反思】
(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是 ;
(2)在化学反应中,相同的反应物因质量比不同可能会导致生成物不同,请另举一列 (写出反应物即可)。
【答案】
【甲组】2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
【乙组】【实验与结论】实验①:<
实验②:中
【交流和反思】
(1)甲组实验生成了Na2SO4,若它显酸性,在此条件下氢氧化钠与硫酸铜反应会生成蓝白色沉淀
(2)碳与氧气
【解析】
试题分析:
【甲组】氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:2NaOH+CuSO4=Na2SO4+ Cu(OH)2↓;
【乙组】【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH<7,硫酸铜溶液呈酸性,猜想Ⅰ成立;
实验②:向盛有硫酸钠溶液的试管中逐滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈中性,猜想Ⅱ不成立;
【交流和反思】
(1)在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生反应会生成不溶于水的蓝白色固体碱式硫酸铜,所以乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立;
(2)碳和充足的氧气反应生成二氧化碳,和不足的氧气反应生成一氧化碳。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】甲班学生做完实验室制备氧气和还原金属氧化物的实验后,剩余物质倒入同一废液缸里。乙班课外兴趣小组同学进行了如图所示的探究。请回答:
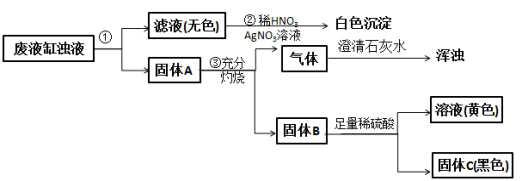
(1)步骤①的操作名称是___________,所用到的玻璃仪器有漏斗、玻璃棒和___________。
(2)由步骤②实验现象推知,甲班同学制取氧气所用的固体反应物是___________(写化学式)。
(3)由步骤④所得溶液加入氢氧化钠可得红棕色沉淀,该反应的化学方程式为______________________。
(4)由步骤③产生的气体判断固体A中一定含有___________(写名称);综合步骤③④现象推理,固体A中还可能含有的物质是______________________(写至少两种物质的化学式)。
(5)根据上述实验和分析判断固体是___________(写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验进行中的现象或实验原理正确的是( )
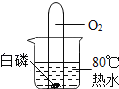
A.白磷始终不燃烧

B.小气球变瘪
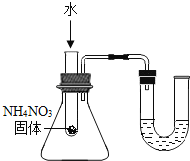
C.U型管内液面左高右低
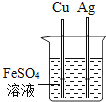
D.验证Fe、Cu、Ag的金属活动性强弱
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
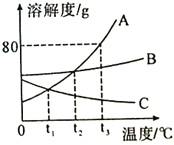
(1)t2℃时,A、B、C三种物质的溶解度大小关系是 .
(2)t3℃时,将30gA物质加入到50g水中,充分溶解后,所得溶液是 (填“饱和”或“不饱和”)溶液.所得溶液溶质质量分数为
(3)室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的并NH4NO3并搅拌,试管内可以观察到的现象是 .
(4)将t2℃时A、B、C三种饱和溶液同时降温至t1℃时,所得溶液中溶质的质量分数的大小关系是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究并设计如下实验.请你将实验设计补充完整.
【猜想假设】
猜想(1):该溶液没有变质,为NaOH溶液.
猜想(2):该溶液全部变质,为 溶液.
猜想(3):该溶液部分变质,为NaOH和Na2CO3的混合溶液.
【查阅资料】Na2CO3溶液呈碱性,氯化钙溶液呈中性.
【设计方案】请你完善下表几组同学探讨的设计方案
实验操作 | 可能出现的现象与结论 | 同学评价 | |
第1组 |
| 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是: . |
第2组 |
| 若产生白色沉淀,反应方程式是: 则猜想(1)不成立. | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立. |
第3组 |
| 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:
|
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:

用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
(1)甲装置中可能发生反应的方程式是 .
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】漳州小吃手抓面,制作时要用发到大树碱,大树碱的主要成分是K2CO3.为了测定大树碱中K2CO3的质量分数,小文同学进行了如下实验;
(1)用托盘天平称取10g大树碱样品,在称量过程中发现天平指针如图所示,则此时应进行的操作是_________.

(2)用量筒量取一定量的水,为了准确量取水的体积,还需要使用的仪器是_________.
(3)把大树碱样品和水加入烧杯中,用玻璃棒搅拌,使大树碱完全溶解,玻璃棒的作用是_________.
(4)向配好的溶液中逐渐加入CaCl2溶液,生成1g沉淀(假设大树碱中其它成分不参与反应,反应的化学方程式为CaCl2+K2CO3═CaCO3↓+2KCl).计算大树碱中K2CO3的质量分数.
(5)小文同学在配制好溶液后,发现纸片上还有残留固体,则计算出的大树碱K2CO3的质量分数_________ (填“偏大”或“偏小”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用甲和乙反应制备丙和丁,其反应的微观示意图如下:
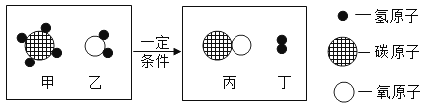
(1)该化学变化中没有发生改变的粒子是______________(填“分子”或“原子”)
(2)写出该反应的化学方程式______________.
(3)该反应中含氢元素的化合物有______________种;反应前后化合价发生可变化的元素是______________(填元素符号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁条在空气中久置表面会变黑。某小组同学设计并进行实验,探究镁条变黑的条件。
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与镁条接触的物质,利用下图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验,并持续观察20天。
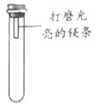
编号 | 主要实验操作 | 实验现象 |
1 | 先充满用NaOH浓溶液洗涤过的空气再加入2mL浓硫酸 | 镁条始终无明显变化 |
2 | 加入2mL NaOH浓溶液 | 镁条始终无明显变化 |
3 | 先加入2mL浓硫酸再通入约4mL CO2 | 镁条始终无明显变化 |
4 | 先加入4mL饱和Na2SO3溶液再充满CO2 | 镁条始终无明显变化 |
5 | 先加入2mL蒸馏水再通入约4mL CO2 | 镁条第3天开始变黑至第20天全部变黑 |
【解释与结论】
(1)实验1和2中,NaOH浓溶液的作用是 (用化学方程式表示)。
(2)实验1的目的是 。
(3)实验3中,试管内的气体主要含有CO2、 。
(4)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是 (填编号)。
(5)由上述实验可推知,镁条变黑的条件是 。
【反思与评价】
(6)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是 。
(7)欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com