
分析 从宏观上分析,纯净物是只有一种物质组成,混合物是至少两种物质组成;从微观上分析,纯净物只有一种分子,而混合物中至少两种分子,单质是由一种元素组成的纯净物,化合物是由不同元素组成的纯净物.
解答 解:A、纯净水是由一种物质组成,属于纯净物,由氢元素和氧元素组成,属于化合物; B、高锰酸钾由一种物质组成,属于纯净物,由三种元素组成,属于化合物;C、大理石主要成分是碳酸钙,还含有其他成分,属于混合物;D、液态氧由氧气一种物质组成,属于纯净物,由氧元素一种元素组成,属于单质.
故答案为:ABD;C;D;AB.
点评 不要从字面上来判断纯净物和混合物,洁净和澄清不能说明该物质是纯净物,应从其组成和构成上来分析解答


科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 中和反应有盐和水生成,所以有盐和水生成的化学反应一定是中和反应 | |
| B. | 因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液 | |
| C. | 酸性溶液的pH都小于7,所以酸溶液的pH也一定小于7 | |
| D. | 因为盐酸和活泼金属反应有气体生成,所以跟盐酸反应有气体生成的物质一定是活泼金属 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 野火烧不尽,春风吹又生 | B. | 春蚕到死丝方尽,蜡炬成灰泪始干 | ||
| C. | 只要功夫深,铁杵磨成针 | D. | 爆竹声中除旧岁,春风送暖入屠苏 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
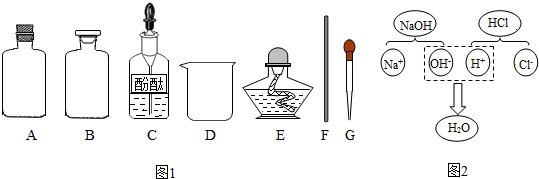
| 实验方案 | 实验步骤 | 现 象 | 结 论 |
| ① | 取样,加入适量的AgNO3溶液 | 出现白色沉淀 | 稀盐酸过量 |
| ② | 取样,加入几滴紫色石蕊试液 | 溶液变红 | 稀盐酸过量 |
| ③ | 取样,加入铁锈粉末 | 红棕色粉末逐渐减少,溶液变成黄色 | 稀盐酸过量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com