
【题目】空气中氧气含量测定的再认识.
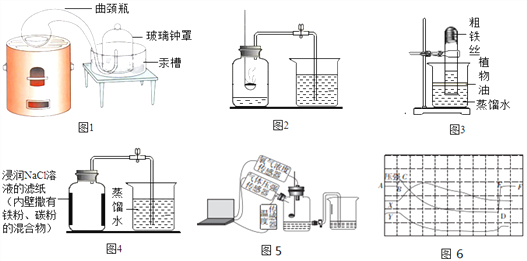
(1)【经典赏析】拉瓦锡用定量的方法研究空气的成分(实验装置如图1).
该实验中选择使用汞的优点有 ____________
A.实验过程中没有污染
B.能将密闭装置内空气中的氧气几乎耗尽
C.在汞槽中起到液封的作用
D.生成的化合物加热分解又能得到汞和氧气
(2)【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的符号表达式________________。图2中集气瓶底部的水的作用为_________。(填字母)
A.吸收有害物质 B.降温,快速冷却 C.保护瓶底
但是用该方法测出的氧气含量常常低于21%。
(3)【提出问题】用该方法测出的氧气含量为什么低于21%?
【进行猜想】①____________;②____________,装置内氧气有剩余;
(4)【实验与交流】为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。其中X曲线表示的是_____(填“温度”或“氧气的浓度”);
【反思拓展】结合X、Y两条曲线,解释如图6中BC段气压变化的原因是_______________;
(5)【实验探究1】已知,铁丝在纯氧中才能燃烧,反应的符号表达式为________________,一般不能在空气中燃烧,因此无法用铁丝代替红磷进行该实验。小明根据铁生锈的原理(铁在常温下可以和氧气、水生成铁锈)来测定空气中氧气的含量,于是进行了实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点____(填字母)。
A.装置内残留的氧气更少
B.反应更彻底,实验结果更准确
C.铁丝生锈比红磷燃烧反应更快
(6)【实验探究2】小明利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:请计算出空气中氧气含量________(计算结果保留一位小数)。相对于实验探究1,实验探究2改进的目的是_______________________。
实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
131mL | 90.0mL | 63.6mL |
(7) 【拓展延伸】铜能与空气中氧气、水、二氧化碳反应生成铜绿[其主要成分为:
Cu2(OH)2CO3]。若将图3中的铁丝换成足量的铜丝,能否比较准确地测定空气中氧气的含量_____________,理由____________(填字母)
A.空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽
B.铜丝反应比铁丝快
C.反应更彻底
【答案】 B、C、D 略 A、B 装置漏气 红磷的量不足 温度 红磷燃烧放热,使瓶内气体受热膨胀,压强变大 略 A 、B 20.2% 加快反应速率 不能 A
【解析】根据所学知识和题中信息知,(1) 拉瓦锡用定量的方法研究空气的成分,该实验中选择使用汞的优点有:①能将密闭装置内空气中的氧气几乎耗尽②在汞槽中起到液封的作用③生成的化合物加热分解又能得到汞和氧气。故选BCD。(2) 实验室常用红磷燃烧的方法测定空气中氧气的含量,红磷燃烧的符号表达式∶P+O2 ![]() P2O5 。图2中集气瓶底部的水的作用为A.吸收有害物质B.降温,快速冷却。(3)【提出问题】用该方法测出的氧气含量为什么低于21%?【进行猜想】①装置漏气;②红磷的量不足,装置内氧气有剩余。(4)【实验与交流】利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。其中X曲线表示的是温度,磷燃烧放热,后冷却。【反思拓展】结合X、Y两条曲线,解释如图6中BC段气压变化的原因是红磷燃烧放热,使瓶内气体受热膨胀,压强变大;(5)【实验探究1】已知,铁丝在纯氧中才能燃烧,反应的符号表达式为∶
P2O5 。图2中集气瓶底部的水的作用为A.吸收有害物质B.降温,快速冷却。(3)【提出问题】用该方法测出的氧气含量为什么低于21%?【进行猜想】①装置漏气;②红磷的量不足,装置内氧气有剩余。(4)【实验与交流】利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。其中X曲线表示的是温度,磷燃烧放热,后冷却。【反思拓展】结合X、Y两条曲线,解释如图6中BC段气压变化的原因是红磷燃烧放热,使瓶内气体受热膨胀,压强变大;(5)【实验探究1】已知,铁丝在纯氧中才能燃烧,反应的符号表达式为∶
Fe+O2 ![]() Fe3O4 。根据铁生锈的原理(铁在常温下可以和氧气、水生成铁锈)来测定空气中氧气的含量,测得的数据计算出空气中氧气的含量为19.13%。【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点∶①装置内残留的氧气更少②反应更彻底,实验结果更准确③操作简单。故选AB。(6)【实验探究2】用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。计算出空气中氧气含量∶90.0mL-63.6mL=26.4ml。
Fe3O4 。根据铁生锈的原理(铁在常温下可以和氧气、水生成铁锈)来测定空气中氧气的含量,测得的数据计算出空气中氧气的含量为19.13%。【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点∶①装置内残留的氧气更少②反应更彻底,实验结果更准确③操作简单。故选AB。(6)【实验探究2】用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。计算出空气中氧气含量∶90.0mL-63.6mL=26.4ml。![]() ×100%=20.2%。相对于实验探究1,实验探究2改进的目的是加快反应速率。(7) 【拓展延伸】铜能与空气中氧气、水、二氧化碳反应生成铜绿[其主要成分为:Cu2(OH)2CO3]。若将图3中的铁丝换成足量的铜丝,不能比较准确地测定空气中氧气的含量,理由是空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽。
×100%=20.2%。相对于实验探究1,实验探究2改进的目的是加快反应速率。(7) 【拓展延伸】铜能与空气中氧气、水、二氧化碳反应生成铜绿[其主要成分为:Cu2(OH)2CO3]。若将图3中的铁丝换成足量的铜丝,不能比较准确地测定空气中氧气的含量,理由是空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽。
点睛∶这是一道实验探究题,通过实验测定空气中氧气的含量。本实验成功的关键①装置气密性良好②磷过量③冷却后测量。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:初中化学 来源: 题型:
【题目】某化学小组同学,用如图所示实验探究质量守恒定律.
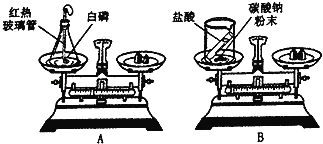
(1)充分反应冷却后,天平仍然平衡的是 (填写字母序号),该反应的化学方程式为 .
(2)由上述实验可知,在化学反应前后,一定不变的 (填数字序号).
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质总质量
(3)红热的铁能与水蒸气反应,放出气体X,同时生成固体Y.X气体靠近火焰点火时,能燃烧或发出爆鸣声.其反应的化学方程式为:3Fe+4H2O![]() 4X+Y.则X的化学式为 ,Y的化学式为 .
4X+Y.则X的化学式为 ,Y的化学式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学家Tim Richard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26)。

请计算:
(1)“小狗烯”的相对分子质量是___________。
(2)“小狗烯”中碳元素和氢元素的质量比____________(填最简整数比)。
(3)含4.8g碳元素的“小狗烯”的质量为_________g?(第(3)小题写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A~F是初中化学常见的六种物质。且A为黑色固体单质,E是可供给动植物呼吸的气体,其余物质都是氧化物。图中“→”表示转化关系,“——”表示反应关系(部分物质和反应条件未标出)。试回答下列问题:
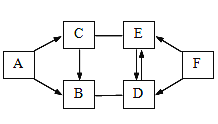
(1)写出下列物质的化学式:A_______,E________;
(2)写出C物质的一种用途_________________;
(3)写出A和B反应的化学反应方程式:_________;
(4)写出由F→D化学反应方程式:_______________;该反应的反应类型是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化硅可用于制造分离膜,利用“膜分离”技术二氧化碳可被浓氨水吸收(如下图)转化为可做氮肥的碳酸氢铵(NH4HCO3)。
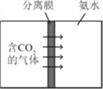
(1)浓氨水属于______________(填“纯净物”或“混合物”)。
(2)NH4HCO3由________种元素组成,其中碳元素和氢元素的质量比为__________。
(3)二氧化硅的化学式为_______。
(4)保持二氧化碳化学性质的最小粒子是_______________(填具体粒子名称),标出二氧化碳中碳元素的化合价__________。
(5)氧离子的结构示意图为![]() ,则X=________,氧离子的离子符号是_______。
,则X=________,氧离子的离子符号是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质存放在烧杯中一段时间后,质量变大且变质的是( )
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰 ⑥稀硫酸.
A.①⑥ B.②③⑤ C.③⑤ D.②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】活动探究一:探究分子运动
如下图所示,烧杯A中是酚酞溶液,烧杯B中是浓氨水。
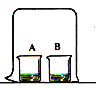
(1)一段时间后,观察到的实验现象是:________________。
(2)对观察到的现象进行解释:易向空气中扩散的是烧杯__________(填A或B)中的物质,这个实验验证了分子是不断运动的特性。
(3)氨气(NH3)在纯净氧气中燃烧,生成空气中含量最多的气体和一种常温下为液体的氧化物,该反应的文字表达式为_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com