
【题目】海洋是人类的巨大资源宝库,试回答下列相关向题:
(1)海水淡化:下图为太阳能海水淡化装置:
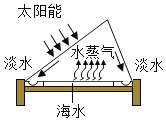
①该海水淡化过程,相当于实验室中的_______(填“蒸发”或“蒸馏”)。
②下列分离混合物的常用方法中,原理与上述方法相同的是______(填序号)。
A 过滤法净化水 B 工业法制氧气 C 活性炭吸附
(2)海水制镁。下图是由海水制备金属镁的工业流程:
![]()
涉及的主要步骤有:①电解熔融的氯化镁②加石灰乳③加盐酸④过滤⑤蒸发结晶
其先后顺序正确的是______
A ②④③⑤① B ②④①⑤③ C ②③④⑤① D ③②④①⑤
(3)海水晒盐:所得粗盐中常含有泥沙等难溶性杂质,可通过溶解、过滤、______等操作去除。这样得到的食盐品体中仍含可溶性杂质![]() ,工业上选用试剂________对其进行除杂.
,工业上选用试剂________对其进行除杂.
(4)海水制“碱”:1926年,我国著名化学家________创立了侯氏制碱法,以管盐为主要原料制取纯碱。生产过程中,先向饱和食盐水中通氨气,再通二氧化碳,涉及的反应原理如下:
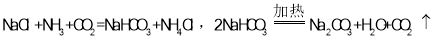
试回答下列问题:
①向饱和食盐水中先通氨气,再通二氧化碳的原因是________.
②纯碱在生活生产中用途广泛。试写出工业上利用纯碱与熟石灰反应制取烧碱的化学方程式:________
【答案】蒸馏 B A 蒸发 碳酸钠 侯德榜 增加二氧化碳的溶解性 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
【解析】
(1)①实验室中采用蒸馏的方法将水净化;
②海水淡化采用不同物质的沸点不同,将物质分离出来,所以工业法制氧气,原理与淡化海水的方法相同;
(2)海水中的氯化镁和氢氧化钙反应生成氯化钙和氢氧化镁沉淀,然后过滤得到氢氧化镁,氢氧化镁和盐酸反应生成氯化镁和水,蒸发得到氯化镁,然后进行电解得到镁,所以先后顺序正确的是:②④③⑤①;
(3)海水晒盐:所得粗盐中常含有泥沙等难溶性杂质,可通过溶解、过滤、蒸发等操作去除;
这样得到的食盐品体中仍含可溶性杂质CaCl2,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,工业上选用试剂碳酸钠对其进行除杂;
(4)侯德榜创立了侯氏制碱法,氨盐水显碱性,容易和二氧化碳反应,所以向饱和食盐水中先通氨气,再通二氧化碳;碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。


科目:初中化学 来源: 题型:
【题目】“见微知著”是化学的一大思维方法,请根据要求回答下列问题。
(1)根据下列粒子的结构示意图回答问题。氧元素和硫元素的化学性质相似的原因是_____。
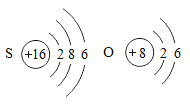
(2)下图是氢氧化钠溶液与盐酸反应的微观示意图和硫酸钠溶液跟氯化钡溶液反应的微观示意图,请根据图示回答。
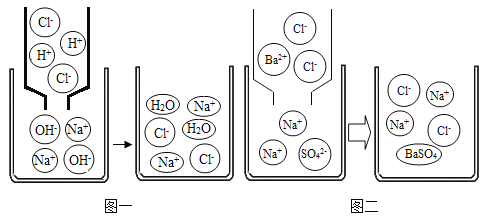
①图一反应的微观实质是____。
②请写出图二的反应方程式___。
③以上两个反应都属于四大基本反应类型中的____,请写出一组属于该类反应且与以上两个反应具有不同特征的反应物____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是
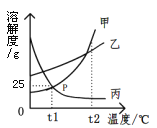
A. P点表示甲、丙两种物质的饱和溶液质量相等
B. t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
C. t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1∶4
D. 将三种物质的溶液从t2℃降至t1℃,溶质质量分数最小的一定是丙物质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜器长期暴露在空气中会生成铜绿(俗称铜锈)。铜锈的主要成分是碱式碳酸铜,其化学式为![]() ,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水。这种黑色固体和无色气体的成分是什么呢?
,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水。这种黑色固体和无色气体的成分是什么呢?
(查阅资料)稀硫酸能与![]() 、
、![]() 等金属氧化物反应,生成盐和水。
等金属氧化物反应,生成盐和水。
(提出猜想)某同学对黑色固体、无色气体的成分做出了以下猜想:
①无色气体为二氧化碳;②黑色固体为氧化铜。
(实验验证)实验装置如图所示。
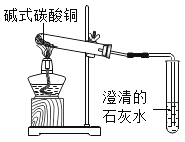
在此实验装置中,大试管的管口略向下倾斜的目的是_____。
(1)若猜想①正确,实验过程中应该看到澄清的石灰水_____,产生此现象的化学方程式是_____;在反应完全停止加热时,针对熄灭酒精灯和把导管移出液面这两步操作,你认为应该先进行的操作是_____。
(2)若猜想②正确,从装置中取下大试管并冷却到室温,然后向大试管中加入足量的稀硫酸,充分振荡,静置后能看到黑色固体消失,溶液由无色变为_____色,发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色粉末,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() ,为确定该白色粉末的成分,同学们进行了有关实验,实验流程和现象如下:
,为确定该白色粉末的成分,同学们进行了有关实验,实验流程和现象如下:
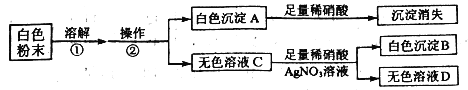
请回答以下问题。
(1)操作②的名称是________,①中发生反应的化学方程式是________。
(2)通过以上实验可知,此白色粉末中一定含有_____;一定不含_____;判断的理由是______。
(3)同学们利用下列两种方案继续对溶液D的成分进行检验,请选择一种方案进行回答。
方案一 | 方案二 | |
操作 | 取少量溶液D,向其中滴加紫色石蕊溶液,观察到溶液变为红色。 | 取少量溶液D,向其中滴加氯化钠溶液,无明显现象;再滴加碳酸钠溶液,观察到先有气泡产生,后产生白色沉淀。 |
结论 | D中所含阳离子一定有上________。 | D中所含阳离子一定有________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表中某元素的一些信息。下列有关该元素的说法正确的是( )
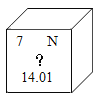
A.该元素的名称是氧元素
B.该元素的一个原子中有7个质子
C.该元素是金属元素
D.该元素的相对原子质量为14.01g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示某化学反应的微观过程,下列有关说法正确的是( )
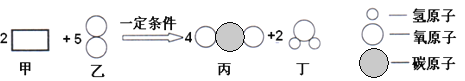
A.甲的化学式为C2H2B.反应物甲的质量等于生成物丁的质量
C.甲和丙均为有机物D.该反应属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黑豆是传统的养生食材,食用9°米醋泡制得到黑豆是一种很好的食疗方法。小明为判断家中的9°米醋含酸量是否合格,拟配制一定质量分数的氢氧化钠溶液进行测定。产品部分信息如图所示。请回答相关问题:

(1)用60g质量分数为10%的氢氧化钠溶液配制成4%的稀溶液,需要水_________mL(水的密度为1g/cm3)。
(2)若9°米醋中的酸均看成是醋酸(化学式:CH3COOH),醋酸中C、H、O三种元素的质量比_________(最简整数比)。
(3)醋酸与氢氧化钠反应的化学方程式为:CH3COOH+NaOH=CH3COONa+H2O,小明取出10mL9°米醋,加入4%的氢氧化钠溶液12g,恰好完全反应。请通过计算判断该产品含酸量是否合格______?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学物质在生活、生产中,以及对人类的健康有着很重要的作用.
(1)碳酸钙可以作为补钙剂,该物质所含酸根的符号是_____.
(2)医用0.9%氯化钠注射液,常含有碳酸氢钠或乳酸钠(C3H5O3Na),其中碳酸氢钠属于___(填“酸”或“碱”或“盐”),乳酸钠中碳元素与氧元素的质量比是_____.
(3)铁锅是有益于人类健康的理想炊具,烹调后留有的铁单质进入胃后,发生反应的化学方程式是____,FeCl2的化学名称是____.
(4)尿素____铵态氮肥(填“属于”、“不属于”),化学式为____,____(填“能”或“不能”)与草木灰等碱性物质混合使用.
(5)奶制品厂收购牛奶时,通过测定含氮量来确定牛奶中蛋白质含量的等级,这里的“氮”是指___.
(6)中和酸性土壤的碱是___;做调味品的盐是___;自来水生产中使用氯气的作用是___;生石灰可作食品干燥剂,其原理是____;活性炭可用来除臭、滤毒等,都是利用它的___.
(7)水参加植物光合作用化学方程式为:6CO2+6H2O![]() 6O2+X,则X的化学式____.
6O2+X,则X的化学式____.
用水鉴别NaOH、NaCl、CaCO3三种固体物质时,能够鉴别出NaOH固体所依据的现象是___.
(8)不法分子常用“铜﹣锌合金”冒充黄金欺骗消费者,请你写出鉴别“铜﹣锌合金”和黄金的两种方法:A____.B____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com