
分析 利用化合价知识对各个反应的化合价进行判断,只要是有化合价变化的反应均是氧化还原反应.利用个反应类型的概念对各基本反应类型中元素的化合价进行分析探讨即可.
解答 解:A、2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO 中镁与氧的化合价均有变化,是氧化还原反应; B、CaO+H2O=Ca(OH)2各元素的化合价均无变化,不是氧化还原反应;C、2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑中氯元素与氧元素的化合价有变化,是氧化还原反应;D、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑中各元素化合价均无变化,不是氧化还原反应;E、H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O中氢元素和铜元素的化合价有变化,是氧化还原反应;F、HCl+NaOH═NaCl+H2O中各元素化合价均无变化,不是氧化还原反应;
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,因此置换反应中一定有化合价的变化,一定属于氧化还原反应;
复分解反应中没有化合价的变化,一定不属于氧化还原反应;
化合反应中可能存在化合价的变化,可能是氧化还原反应;
分解反应中可能存在化合价的变化,可能是氧化还原反应;
故答案为:一定属于氧化还原反应;一定不属于氧化还原反应;可能是氧化还原反应;可能是氧化还原反应.
点评 此题是借助信息对氧化还原反应的探讨,主要是利用化合价知识对氧化还原反应的再认识,属于信息给予题的范畴.


科目:初中化学 来源: 题型:解答题
| 实验编号 | 铝铜合金质量(g) | 加入稀硫酸质量(g) | 生成H2质量(g) |
| 实验1 | 20 | 200 | 1 |
| 实验2 | 20 | 300 | 1.5 |
| 实验3 | 20 | 400 | 2 |
| 实验4 | 20 | 500 | 2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
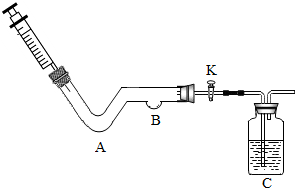 某化学小组同学利用如图所示装置进行实验.
某化学小组同学利用如图所示装置进行实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe、Ag | B. | Fe、Zn | C. | Zn、Ag | D. | Zn、Ag、Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
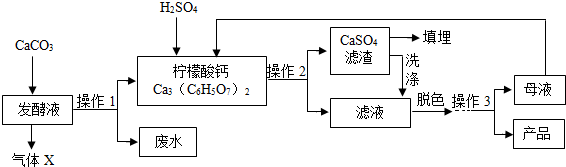
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | … |
| 溶解度/g | 96 | 118 | 146 | 183 | 216 | … |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验次数 | 每次产生的CO2的质量/g |
| 第一次先逐滴滴加稀盐酸100g | 0 |
| 第二次再逐滴滴加稀盐酸100g | 8.8 |
| 第三次再逐滴滴加稀盐酸100g | 0 |
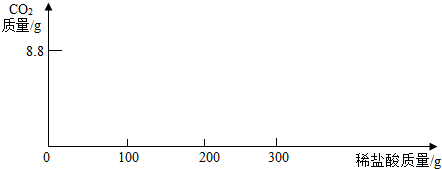
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素属于有机物,由碳、氢、氧3个元素组成 | |
| B. | 青蒿素由15个碳原子、22个氢原子、5个氧原子构成 | |
| C. | 甲醇、乙醇在空气中充分燃烧一定都能生成二氧化碳和水 | |
| D. | 青蒿素中碳、氢、氧元素的质量比为15:22:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
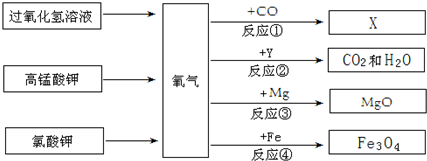
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com