
分析 (1)根据氢氧化钠的性质和用途进行分析;
(2)根据经过操作②后分出了溶液和固体进行分析;
(3)根据氯化钡、碳酸钠所除去的离子和除杂质的原则进行分析;
(4)根据反应物、生成物以及反应条件书写方程式;
(5)根据该反应的流程图进行分析;
(6)加入过量Na2CO3溶液的目的是为了除去剩余的氯化钡和氯化钙;先过滤而后加盐酸溶液,其理由是防止沉淀溶于盐酸.
(7)加入氢氧化钠是为了除去氯化镁,加入氯化钡是为了除去硫酸钠,加入碳酸钠是为了除去剩余的氯化钡和氯化钙.
解答 解:(1)A、氢氧化钠可以和油污反应生成硬脂酸钠而将油污溶解,故A正确;
B、氢氧化钠极易溶于水,并且放出大量的热,故B正确;
C、石蕊遇氢氧化钠溶液变蓝色,故C错误;
D、氢氧化钠具有吸水潮解的性质,所以可以干燥某些气体,故D正确;
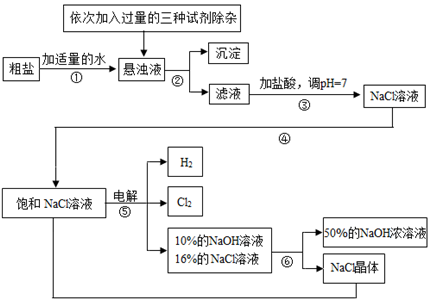
(2)过滤是将固体和液体进行分离的一种操作,故操作②为过滤;
(3)将BaCl2溶液改用硝酸钡溶液,会引入硝酸根杂质;氢氧化钡能与氯化镁和硫酸钠反应,所以,可以用氢氧化钡溶液代替BaCl2溶液可达到同样的目的;
(4)饱和的氯化钠在通电的条件下生成氯化钠、氢气和氯气,故化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(5)根据装置图可以看出,电解反应后的溶液中依然存在氯化钠,氯化钠蒸发变成饱和状态时又可以电解,所以,该流程中可以循环利用的物质是氯化钠.
(6)加入过量Na2CO3溶液的目的是为了除去剩余的氯化钡和氯化钙;先过滤而后加盐酸溶液,其理由是防止沉淀溶于盐酸.
(7)加入氢氧化钠是为了除去氯化镁,加入氯化钡是为了除去硫酸钠,加入碳酸钠是为了除去剩余的氯化钡和氯化钙,顺序加反后,剩余的氯化钡也就成了杂质,其中加入氢氧化钠和氯化钡的顺序可以颠倒,所以加入顺序是氯化钡、碳酸钠、氢氧化钠.
故填:(1)C; (2)过滤; (3)引入硝酸银新杂质;氢氧化钡;(4)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑; (5)NaCl;(6)除去剩余的氯化钡和氯化钙;防止沉淀溶于盐酸;(7)氯化钡、碳酸钠、氢氧化钠.
点评 本题主要考查了粗盐提纯时的物质的除杂和净化,在除杂质时不要引入新的杂质,了解混合物的分离和除杂的方法.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在空气中打开浓盐酸的瓶盖冒白雾 | |
| B. | 向滴有酚酞溶液的蒸馏水中加入稀硝酸,溶液显红色 | |
| C. | 久置于空气中的熟石灰,加入稀盐酸会有气体产生 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 铁制品在我们家庭中应用广泛,现有从洗澡间拆下的两根生锈的铁管A管里面生了很多锈,B外面生锈严重,你根据所学知识回答问题:
铁制品在我们家庭中应用广泛,现有从洗澡间拆下的两根生锈的铁管A管里面生了很多锈,B外面生锈严重,你根据所学知识回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
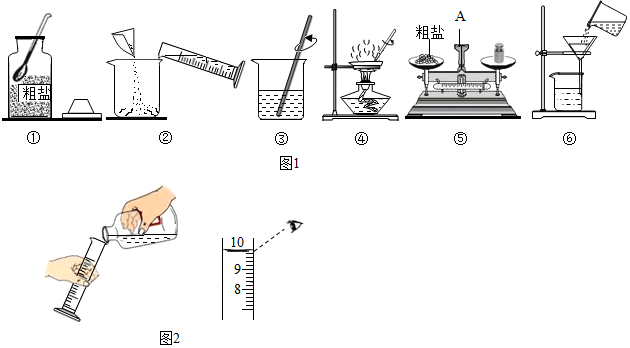
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
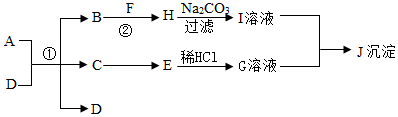
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com