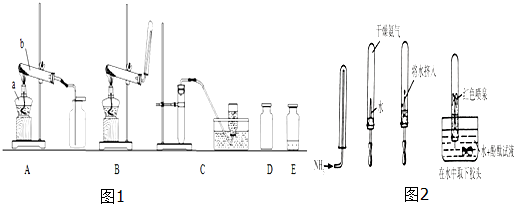
某化学兴趣小组同学在回收废旧电池的同时,开展了如下的实验探究.
【查阅资料】废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.
【实验1】废干电池的拆卸与处理
(1)兴趣小组同学将废旧干电池卸下的锌筒、碳棒冲洗干净,备用.
(2)将铜帽放入盐酸中,除去锈污,冲洗备用.
【实验2】检验废干电池筒内黑色固体中MnO
2的存在
兴趣小组同学设计了如图所示的实验:
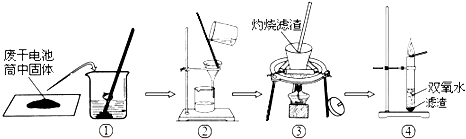
(1)操作②中过玻璃棒的作用是
.
(2)操作③灼烧黑色滤渣时,会产生一种能使澄清石灰水变浑浊的气体,该气体为
.
(3)操作④试管中产生的气体能使带火星木条复燃,该气体为
.
(4)由此得出结论:滤渣中除含有
外,还含有黑色粉末
.
【实验3】利用回收锌皮制取氢气及相关探究
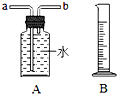
(1)用锌皮和稀硫酸制取氢气.用适当的发生装置,采用排水法收集并测定氢气的体积(如图),气体从装置A导管口
(填“a”或“b”) 进,选用仪器B测量排出水的体积,仪器B名称是
.
(2)探究影响锌与稀硫酸反应快慢的因素.反应过程中用前10min 内
收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表4组实验,获得数据如表.
| 实验编号 | 试剂[来源:学科网ZXXK] | 前10 min内产生的
氢气体积(mL)[来源:学|科|网Z|X|X|K] |
| 锌的纯度 | 稀硫酸的体积和浓度 |
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 mL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
【数据分析】
①比较实验a和实验b得到的结论是:
.
②为了研究硫酸浓度对反应快慢的影响,需比较实验
(填实验编号).
③探究影响该反应快慢的因素,还需控制的条件是:
(举一例即可).
【实验4】探究经处理干净的二氧化锰在氯酸钾分解反应中的催化作用
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热.
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体.
(3)再将残留固体经溶解、过滤、洗涤、干燥、称量,得到5.5g黑色固体.
【数据分析】
①该实验说明:二氧化锰在氯酸钾分解反应前后,
不变.
②完全反应后制得氧气的质量是
g.(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后各生成物的质量总和)
【实验反思】
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较
的大小.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案