
| 实验一 | 实验二 |
 |  |
| 实验三 | 实验四 |
 |  |

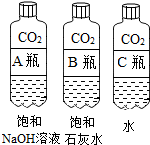
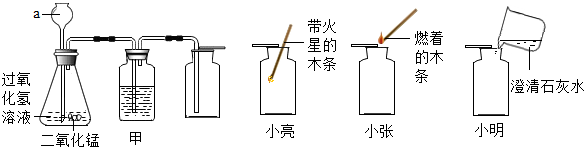
分析 (1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生的反应是:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,对比A瓶与C瓶的实验现象,可证明CO2能与NaOH发生反应;(2)根据二氧化碳溶于水生成碳酸进行分析;
(3)根据硝酸钾、氯化钠的溶解性进行回答;
(4)酸类因为溶于水时电离出的阳离子相同,有相同的化学性质,又因为溶于水时电离出的阴离子或酸根离子不同,其性质也存在差异;
解答 解:(1)用对比实验方法探究二氧化碳的性质:实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生的反应是:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,对比A瓶与C瓶的实验现象,可证明CO2能与NaOH发生反应;故答案为:Ca(OH)2+CO2=CaCO3↓+H2O;C;
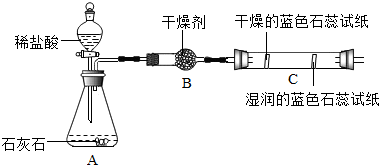
(2)实验二观察到C装置中发生的现象是:干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色;因为二氧化碳溶于水生成碳酸;故答案为:干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色;
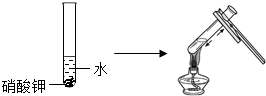
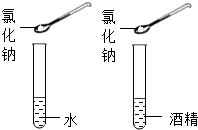
(3)硝酸钾在低温不溶,加热继续溶解,说明物质的溶解性与温度有关;氯化钠不溶于酒精,而溶于水.故实验呈现的不同现象能说明物质的溶解性与溶剂种类有关;故填:温度;溶剂种类;
(4)酸类因为溶于水时电离出的阳离子相同,有形同的化学性质,又因为溶于水时电离出的阴离子或酸根离子不同,其性质也存在差异;氯化钡溶液与硫酸溶液反应的条件是钡离子和硫酸根离子产生硫酸钡沉淀,故该反应的实质是:Ba2++SO42-=BaSO4↓;故填:ABD;阴离子或酸根离子;Ba2++SO42-=BaSO4↓;
点评 本题考查知识面较广,注意通过给出微粒的模型,考查学生的知识迁移能力和对复分解反应的应用能力.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 主食 | 米饭 馒头 |
| 副食 | 红烧肉 鸡蛋 豆腐汤 |
| 饮料 | 纯净水 可乐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.
通过化学启蒙学习,同学们对组成万物的基本物质有了进一步了解.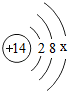 ,其中x=4.
,其中x=4.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
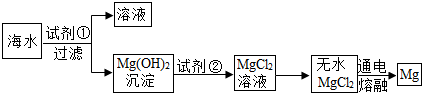
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
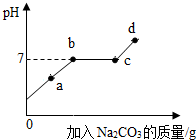 烧杯中盛有CaCl2和HCl的混合溶液,向其中滴加Na2CO3溶液,烧杯中溶液的pH与滴加溶液的质量关系如图所示.下列说法错误的是( )
烧杯中盛有CaCl2和HCl的混合溶液,向其中滴加Na2CO3溶液,烧杯中溶液的pH与滴加溶液的质量关系如图所示.下列说法错误的是( )| A. | a点的溶质为HCl、NaCl | |
| B. | ab段反应产生大量气泡 | |
| C. | bc段反应的方程式为CaCl2+Na2CO3═2NaCl+CaCO3↓ | |
| D. | 取d点溶液滴加酚酞试液,溶液显红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
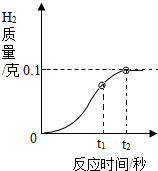 为测定某黄铜中铜的质量分数,小欣进行以下实验:取10.0g黄铜样品与足量稀盐酸充分反应,产生的氢气与反应时间的函数关系如图
为测定某黄铜中铜的质量分数,小欣进行以下实验:取10.0g黄铜样品与足量稀盐酸充分反应,产生的氢气与反应时间的函数关系如图查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com