
| 127 |
| 214 |


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:初中化学 来源: 题型:
| A、卟啉铁由76个原子构成 |
| B、1个卟啉铁分子中含有34个碳原子 |
| C、卟啉铁中含有6种元素 |
| D、“缺铁性贫血”中的“铁”指铁元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
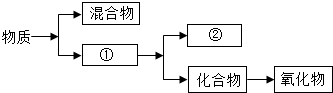 如图是关于物质的分类:
如图是关于物质的分类:查看答案和解析>>
科目:初中化学 来源: 题型:
| A、红磷在空气中燃烧,产生大量烟雾 |
| B、镁在空气中燃烧,发白光,生成白色固体氧化镁 |
| C、蜡烛在氧气中燃烧,发出红光 |
| D、氢气在空气中燃烧产生淡蓝色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、制取二氧化碳气体前,先检查装置的气密性 |
| B、点燃氢气前,先检查氢气的纯度 |
| C、用嘴吹灭酒精灯的火焰 |
| D、做铁丝在氧气中燃烧的实验前,先在集气瓶底加入少量细沙 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 1 |
| 5 |
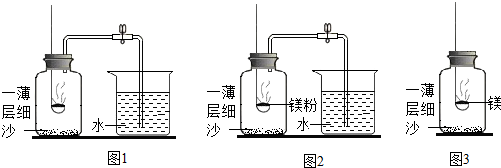
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com