
| A. | 第一次反应停止后,B剩余9g | B. | 第二次反应后,C的质量为10g | ||
| C. | 反应中A和B的质量比为3:2 | D. | 第二次反应消耗的C的质量为4g |
分析 若增加10gA,则反应停止后,原反应物中只余C,据此可确定参加反应的A与B的质量关系;A、B、C三种物质各15g,它们化合时只能生成30g新物质D,据此又可确定参加反应的A、B、C的质量及质量比关系;从而又可确定参加第二次反应的A、B、C的质量及反应结束后生成D的质量.
解答 解:若增加10gA,则反应停止后,原反应物中只余C,说明参加第二次反应的A的质量为25克,B的质量为15克,A与B参加反应的质量比为5:3;A、B、C三种物质各15g,它们化合时只能生成30g新物质D,说明参加第一次反应的A的质量为15克,B的质量为9克,根据质量守恒定律可知参加第一次反应的C的质量为6克,则A、B、C参加反应的质量比为5:3:2,则第二次参加反应的C的质量为4克,生成D的质量为50克.
A、参加第一次反应的B的质量为9克,剩余6克.故A不正确;
B、第二次参加反应的C的质量为4g,故第二次反应后,C的质量为15g-6g-4g=5g.不正确;
C、反应中A与B的质量比为5:3.故C不正确;
D、第二次参加反应的C的质量为4g.故D正确.
故选D.
点评 质量守恒定律是自然界的普遍规律,它揭示了化学反应中反应物和生成物之间的质量关系,质量守恒定律的应用是中考考查的重点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 4.08g | B. | 8.17g | C. | 12.26g | D. | 16.34g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 18gMg、18gCu | B. | 20gCaO、20gCaCO3 | ||
| C. | 10gAgNO3溶液、5gCu(OH)2 | D. | 4gMg(OH)2、8.4gMgCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 甲、乙、丙三种物质的溶解度曲线如图所示,据图回答:
甲、乙、丙三种物质的溶解度曲线如图所示,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
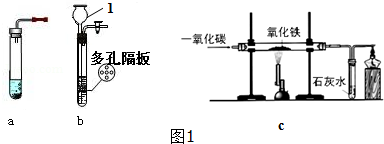 如图1所示装置制取氢气,试回答下列问题:
如图1所示装置制取氢气,试回答下列问题:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 元素符号 | H | He | Li | Be | B[ | C | N | O | F |
| 原子序数 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 元素符号 | Ne | Na | Mg | Al | Si | P | S | Cl | Ar |
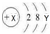 ,当X-Y=8时,该粒子的符号为S2-.
,当X-Y=8时,该粒子的符号为S2-.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分解反应不可能生成化合物,只能生成单质 | |
| B. | 化合反应的生成物一定是化合物 | |
| C. | 矿泉水中含有多种不同的元素,所以矿泉水是化合物 | |
| D. | 混合物的组成中肯定含多种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
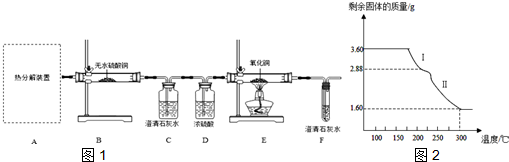
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com