
下列物质属于化石燃料的是( )
A. 煤 B. 酒精 C. 木材 D. 一氧化碳
A 【解析】A、煤、石油和天然气属于三大化石燃料,正确;B、酒精属于可再生能源,不是化石燃料,错误;C、木材不是化石燃料,错误;D、一氧化碳是无机燃料,不是化石燃料,错误。故选A。 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案科目:初中化学 来源:内蒙古2018届九年级下学期模拟考试(三)化学试卷 题型:单选题
下列图中能正确反映其对应关系的是 ( )

A. 向氢氧化钠溶液中不断加水,溶液pH与加入水的质量的关系
B. 向盛有氧化铜的烧杯中加入稀盐酸至过量,生成氯化铜质量与加入稀盐酸质量的关系
C. 一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
D. 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液,生成沉淀与加入氢氧化钠溶液的质量关系
C 【解析】试题分析:A中向氢氧化钠溶液中不断加水,溶液pH变小,但不会变成中性溶液或酸性溶液,A错误;反应开始前没有氯化铜,故氯化铜的质量应从0开始,B错误;C中锌与硫酸反应生成硫酸锌和氢气,溶液的质量会增加,反应完全后溶液的质量保持不变,C正确;D中有加热的氢氧化钠溶液先与硫酸反应,再与硫酸铜反应,故一段时间后才会生成沉淀,D错误。故选C。查看答案和解析>>
科目:初中化学 来源:山东省聊城市莘县2018届九年级第二次模拟考试化学试卷 题型:单选题
把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间,测得反应后各物质的质量如下,则下列说法中错误的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量(g) | 7.6 | 2.0 | 0.2 | 0 |
反应后的质量(g) | 3.2 | X | 5.8 | 0.4 |
A. X=0.4 B. 丁一定是单质
C. 甲和乙是反应物 D. 反应中的甲、丙发生改变的质量比是11:14
D 【解析】根据表格可知各物质反应前后的质量变化。甲反应前为7.6g,反应后为3.2g,质量减少了4.4g,属反应物;丙反应前为0.2g,反应后为5.8g,质量增加了5.6g,属生成物;丁反应前质量为0,反应后质量为0.4g,质量增加了0.4g,属生成物;根据质量守恒定律化学反应前后物质的总质量不变可知乙是反应物,反应了1.6g。该反应表示为:甲+乙→丙+丁。A、乙反应了1.6g, 故X=2...查看答案和解析>>
科目:初中化学 来源:广东省2017-2018学年八年级下学期第二次月考化学试卷 题型:实验题
实验室按下图所示装置制取CO2,并检验CO2的性质。试回答以下问题:


(1)实验开始前,先应检查装置A的______________。
(2)用装置A来制取CO2,所用的药品是_____和_____(两空均填写主要成分化学式)
(3)若要用装置B鉴定CO2,在B中应盛放的试剂是(填写主要成分的化学式)_________,当将标①和②的导管口连接时,B中看到的实验现象是___________。
(4)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是_____________,当将标①和③的导管口连接时,C中看到的实验现象是___________。
(5)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是在______(选填“上层”或“下层”)的蜡烛先熄灭。
(6)实验室用装置E来收集二氧化碳时,二氧化碳应从___________(填“a”或“b”)端通入。
气密性 CaCO3 HCl Ca(OH)2 澄清的石灰水变浑浊 紫色石蕊溶液 石蕊溶液变红 下层 a 【解析】制取CO2,并检验CO2的性质。(1)实验开始前,先应检查装置A的气密性,凡是制取气体装置,反应前都必须检查装置的气密性。(2)用装置A来制取CO2,所用的药品是CaCO3和HCl。(3)若要用装置B鉴定CO2,在B中应盛放的试剂是Ca(OH)2,二氧化碳与Ca(OH)2 反应生成白...查看答案和解析>>
科目:初中化学 来源:广东省2017-2018学年八年级下学期第二次月考化学试卷 题型:单选题
下列各种现象与可燃物着火点无关的是
A. 酒精灯用火柴点燃,而煤须用其他易燃物引燃
B. 白磷存放在冷水中能防止自燃
C. 把盛有水的小纸船放在酒精灯上加热,小纸船没有燃烧起来
D. 电器着火时常用沙土扑灭
D 【解析】A、酒精灯用火柴点燃,而煤须用其他易燃物引燃,酒精着火点降低,煤着火点较高;B、白磷存放在冷水中能防止自燃,白磷着火点降低;C、把盛有水的小纸船放在酒精灯上加热,小纸船没有燃烧起来,没有达到小纸船燃烧的着火点;D、电器着火时常用沙土扑灭,防止触电事故发生。 点睛∶任何可燃物燃烧在与空气成分接触的同时温度必须达到可燃物的着火点。查看答案和解析>>
科目:初中化学 来源:四川省南充名校2018届九年级中考适应性联考化学试卷 题型:科学探究题
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
(提出问题)白色固体是什么物质?
(做出猜想)小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:__________________;猜想三:Ca(OH)2。
他的依据是____________________。
(交流反思)经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:_______________。
(进行实验)
(1)取少量白色固体放入试管中,滴加稀盐酸,没有观察到____________,证明猜想二不成立。
(2)取少量白色固体加入到水中,静置后取上层清液,___________,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为:_____________。
结论:白色固体是Ca(OH)2。由碳化钙与水反应制取乙炔的化学方程式为___________
(拓展应用)已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的发生装置是_____,收集装置是_________(选填图中装置序号)。

查看答案和解析>>
科目:初中化学 来源:四川省南充名校2018届九年级中考适应性联考化学试卷 题型:单选题
下图为A、B、C三种固体物质(不含结晶水)的溶解度曲线。下列有关说法错误的是

A. t1℃C三种物质中B物质的溶解度最大
B. t2℃三种物质的饱和溶液中,溶质的质量分数最大的是A
C. 可用降低温度的方法使t2℃时C的饱和溶液变为不饱和溶液
D. 将t2℃A、B、C三种物质的饱和溶液降温到t1℃,溶质的质量分数的大小关系是B>A=C
D 【解析】A、由溶解度曲线可知:t1℃三种物质中B物质的溶解度大,不符合题意;B、t2℃三种物质的饱和溶液中,溶质的质量分数最大的是A,不符合题意;C、可用降低温度的方法使t2℃时C的饱和溶液变为不饱和溶液正确,因为C的溶解度随温度的升高而减少,不符合题意;D、由溶解度曲线可知:将t2℃A、B、C三种物质的饱和溶液降温到t1℃,溶质的质量分数的大小关系是:B>A>C,故错误,符合题意。故选...查看答案和解析>>
科目:初中化学 来源:湖北省随州市高新区四校2018届九年级下学期第三次段考理科综合化学试卷 题型:单选题
如图是a、b、c三种固体物质(都不含结晶水)的溶解度曲线,下列说法中正确的是( )
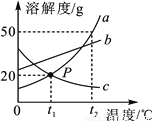
A. t2 ℃时,向50克水中加入50克a,充分溶解后可得到100克溶液;
B. t 1 ℃时,c的饱和溶液中溶质的质量分数为20% ;
C. t2 ℃时,等质量a、b、c三种饱和溶液中分别降温到t 1 ℃,所得溶液中溶剂的质量大小关系式c>b>a;
D. 分别将t2 ℃时a、b、c的饱和溶液降温至t 1 ℃,则所得的三种溶液中溶质的质量分数大小关系是b>a=c;
C 【解析】根据所学知识和题中信息知,A、t2 ℃时,a物质溶解度是50g,向50克水中加入50克a,充分溶解后可得到50g+25g=75g溶液,故A错误;B、t 1 ℃时,c物质溶解度是20g,c的饱和溶液中溶质的质量分数为×100%=16.7%,故B错误;C、t2 ℃时,a、b、c三种溶解度大小关系是等质量a>b>c,三种饱和溶液中分别降温到t 1 ℃,所得溶液中溶剂的质量大小关系式c>...查看答案和解析>>
科目:初中化学 来源:江苏省南通市2018届九年级中考模拟考试三化学试卷 题型:null
下列排序正确的是( )
A. 空气中物质含量:
B. 溶液pH:
C. 金属活动性顺序:
D. 硫元素质量分数:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com