
| A. | N2 | B. | O2 | C. | CO2 | D. | H2O |
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步 骤 | 现 象 | 结 论 |
| 往大小相同的纯锌片和纯铁片中分别加入等质量、等溶质质量分数的稀盐酸 | 锌片产生气泡快 铁片产生气泡慢 | 金属锌的活动性大于铁的活动性 |
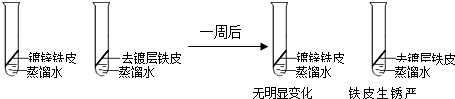
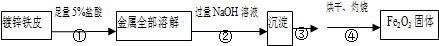
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用燃着的木条区别N2和CO2 | |
| B. | 区别CO和CO2可分别通入紫色石蕊溶液 | |
| C. | 除去CO2中混有少量的CO可通过点燃CO气体 | |
| D. | 除去CO中混有少量的CO2可通过灼热的CuO |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\stackrel{0}{H}$2:氢气中氢元素的化合价为0 | B. | 2CO2:两个二氧化碳分子 | ||
| C. | 2N:2个氮原子 | D. | FeSO4:硫酸铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 6 | D. | 8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
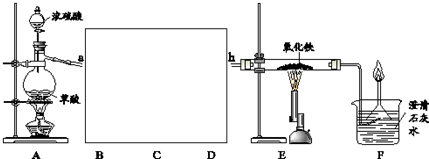
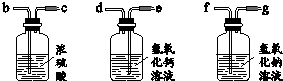
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com