
| A. | 该物质由三种元素组成 | B. | 该物质由10个原子构成 | ||
| C. | 该物质中硅元素的化合价为+6价 | D. | 各元素的质量比为23:27:56:96 |
分析 A、根据NaAlSi2O6的元素组成进行分析判断.
B、根据NaAlSi2O6的微观构成进行分析判断.
C、根据在化合物中正负化合价代数和为零,结合化学式进行判断.
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答
解答 解:A、NaAlSi2O6是由钠、铝、硅、氧四种元素组成的,故选项说法错误.
B、NaAlSi2O6是由NaAlSi2O6分子构成的,1个NaAlSi2O6分子由10个原子构成,故选项说法错误.
C、钠元素显+1价,铝元素显+3价,氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+(+3)+2x+(-2)×6=0,则x=+4价,故选项说法错误.
D、NaAlSi2O6中钠元素、铝元素、硅元素、氧元素质量比为23:27:28×2:16×6=23:27:56:96,故D说法正确.
故选:D
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | 玻璃态水不属于氧化物 | |
| B. | 玻璃态水分子不运动 | |
| C. | 玻璃态水和普通水的化学性质相同 | |
| D. | 玻璃态水分子间隔比普通水的分子间隔小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
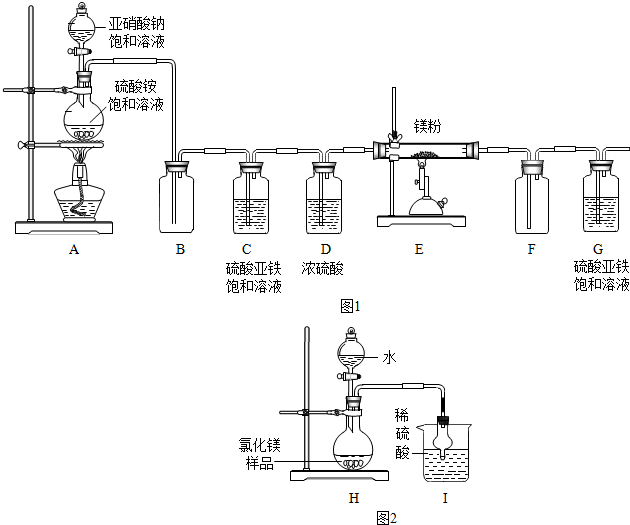
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化亚铁和盐酸 | B. | 铁和盐酸 | ||
| C. | 氧化亚铁和盐酸 | D. | 氢氧化铁和盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食品添加剂有害人体健康,应禁止使用 | |
| B. | 购物时减少使用或不用塑料袋,是为了减少“白色污染” | |
| C. | 为防止土壤和水体富营养化,应禁止使用化肥与农药 | |
| D. | 不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 给烧杯加热时,要垫上石棉网 | |
| B. | 给试管里的液体加热,液体体积不超过试管容积的三分之一 | |
| C. | 给试管里的液体加热时,不让试管口对着自己和旁人 | |
| D. | 实验中剩余的药品都要放回原试剂瓶 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
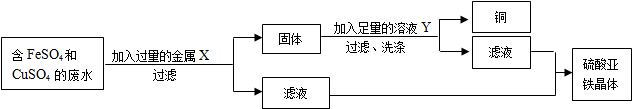
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验目的 | 实验设计 | |
| A | 除去铜粉中混有的少量铁粉 | 加入适量的稀盐酸,再过滤 |
| B | 鉴别浓盐酸和浓硫酸 | 分别用玻璃棒蘸取点在滤纸上 |
| C | 除去稀盐酸中混有的少量的硫酸 | 加入过量的BaCl2溶液,再过滤 |
| D | 鉴别蒸馏水和矿泉水 | 加入肥皂水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com