

分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气进行分析;
(3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,C装置利用压强差可以实现固体和液体的分离,除去氯化氢常用饱和碳酸氢钠溶液,浓硫酸有吸水性,洗气应该是长进短出进行分析;
(4)根据化学方程式和题中所给的数据进行计算.
解答 解:(1)通过分析题中所指仪器的作用可知,①是长颈漏斗;
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑;
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,C装置利用压强差可以实现固体和液体的分离,优点是:可以随时控制反应的发生和停止,除去氯化氢常用饱和碳酸氢钠溶液,浓硫酸有吸水性,洗气应该是长进短出,所以正确的顺序是d→c→a→b,故选:C;
(4)49g×10%=4.9g
设最多生成氢气的质量为x
Zn+H2SO4=ZnSO4+H2↑
98 2
4.9g x
$\frac{98}{4.9g}$=$\frac{2}{x}$
x=0.1g
答:最多生成氢气的质量是0.1g.
故答案为:(1)长颈漏斗;
(2)2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑;
(3)CaCO3+2HCl=CaCl2+CO2↑+H2O,可以随时控制反应的发生和停止,C;
(4)最多生成氢气的质量是0.1g.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:实验探究题
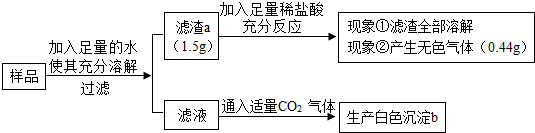
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A化学与生活 | B化学与安全 |
| ①用洗涤剂去除油污 ②用镶有金刚石的玻璃刀裁玻璃 ③用生石灰作食品干燥剂 | ①炒菜锅着火可以用锅盖盖火 ②在室内一盆水能防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 |
| C化学与资源 | D化学与发现 |
| ①防止金属腐蚀是保护金属资源的途径之一 ②煤、石油、天然气是可再生能源 ③海洋中蕴藏着丰富的化学资源 | ①波义耳发现酸碱指示剂 ②拉瓦锡发现元素周期律并编制元素周期表 ③门捷列夫发现空气的组成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
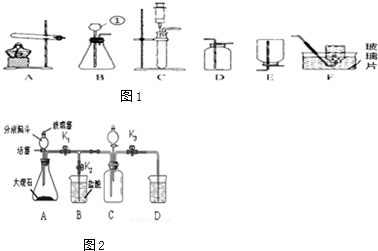
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
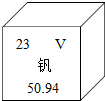 钒被誉为“合金的维生素”,钒元素的相关信息如图所示.下列有关钒的说法不正确的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如图所示.下列有关钒的说法不正确的是( )| A. | 属于金属元素 | B. | 原子序数为23 | ||
| C. | 原子核外电子数为23 | D. | 相对原子质量为50.94g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
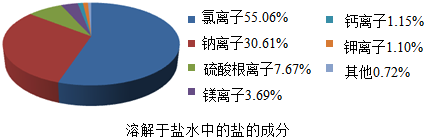
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | Fe3O4 | B. | Fe3O4和Fe2O3 | ||
| C. | Fe和Fe2O3且质量比为7:20 | D. | FeO和Fe2O3且质量比为9:20 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛 | B. | 焦油 | C. | 尼古丁 | D. | 一氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com