

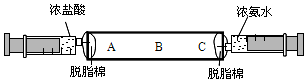
分析 向试管中加入药品前应先检验:检查装置的气密性;长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳可以用浓硫酸干燥,用F收集气体时气体应从长管进入,因为二氧化碳的密度比空气的密度大;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.
解答 解:(1)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;向试管中加入药品前应先检验:检查装置的气密性;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;A;检查装置的气密性;
(2)长颈漏斗方便加液体药品,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳可以用浓硫酸干燥,用F收集气体时气体应从长管进入,因为二氧化碳的密度比空气的密度大;故答案为:长颈漏斗;E;浓硫酸;d;
(3)设计D方案检验产生的气体是什么,则D方案中的仪器和药品分别是:试管(或烧杯或广口瓶等);澄清石灰水;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:试管(或烧杯或广口瓶等);澄清石灰水;CO2+Ca(OH)2═CaCO3↓+H2O;
(4)图中C的现象是:首先观察到有大量气泡产生,试管内液面逐渐下降至脱离锌粒,长颈漏斗的液面升高,反应停止;故答案为:首先观察到有大量气泡产生,试管内液面逐渐下降至脱离锌粒,长颈漏斗的液面升高,反应停止;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、检查装置的气密性和气体的检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


科目:初中化学 来源: 题型:推断题
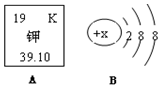 钾在人体内起着调节体液平衡的作用,如图A是钾元素在元素周期表中的相关信息.
钾在人体内起着调节体液平衡的作用,如图A是钾元素在元素周期表中的相关信息.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁条可在空气中燃烧,故铁丝也可在空气中燃烧 | |
| B. | 金刚石很硬,故石墨也很硬 | |
| C. | 氢氧化铝可治疗胃酸过多,故氢氧化钠也可用于治疗胃酸过多症 | |
| D. | 生铁比纯铁硬,故黄铜比纯铜硬 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
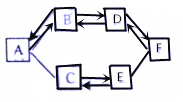 如图是初中化学几种常见物质间的反应及转化关系,A物质是气体,C是红色固体,D广泛用于玻璃、造纸和洗涤剂的生产,下图中“-”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质.请回答:
如图是初中化学几种常见物质间的反应及转化关系,A物质是气体,C是红色固体,D广泛用于玻璃、造纸和洗涤剂的生产,下图中“-”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2MoO4中钠与氧的元素质量比为23:17 | |
| B. | Na2MoO4中含有4个氧原子 | |
| C. | Na2MoO4中钼元素的化合价是+6价 | |
| D. | Na2MoO4中钼元素质量分数最小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 亮氨酸中含有氧分子 | B. | 亮氨酸属于有机高分子化合物 | ||
| C. | 亮氨酸由四种元素构成 | D. | 亮氨酸中氢元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
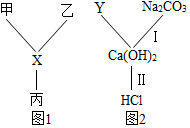 通过学习,我们认识了酸、碱、盐的化学性质,用所学知识回答.
通过学习,我们认识了酸、碱、盐的化学性质,用所学知识回答.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com