
| 硫酸(500mL) 品名 硫酸 化学式 H2SO4 相对分子质量98 密度 1.84g/cm3 质量分数98%(1)该试剂瓶中硫酸溶液的质量是 (2)某固体物质由氯化钠和氯化钡组成,取32.8g该固体混合物完全溶于水,并逐滴加入上述20%的稀硫酸,产生沉淀的质量与加入稀硫酸的质量有如图所示关系,计算32.8g固体混合物中氯化钠和氯化钡的质量.(H2SO4+BaCl2═BaSO4↓+2HCl) 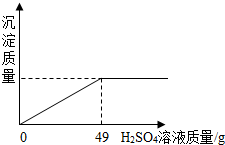
分析:(1)硫酸的质量等于硫酸的体积与密度乘积.根据加水质量前后溶液中溶质硫酸的质量不变,计算出加水稀释时所用98%的浓硫酸与水的质量比; (2)氯化钠和氯化钡的混合溶液中只有氯化钡可与硫酸反应生成硫酸钡沉淀和氯化氢,由反应的曲线图可得知,加入稀硫酸49g时反应恰好完成;利用所加硫酸的质量,根据反应的化学方程式计算出参加反应的氯化钡的质量,氯化钠的质量=32.8g固体混合物-氯化钡的质量. 解答:解: (1)①溶液的质量等于溶液的体积与密度的乘积. 浓硫酸的质量=500mL×1.84g/mL=920g ②设稀释成20%的稀硫酸时所用98%的浓硫酸与水的质量比a:b a g×98%=(a g+b g)×20% 解得a:b=10:39 (1)①920g ②10:39 (2)加入的稀硫酸刚好使沉淀最大量时,参加的反应的硫酸的质量:49g×20%=9.8g 设32.8g固体中含有BaCl2的质量为x BaCl2+H2SO4=BaSO4↓+2HCl 208 98 73 x 9.8g y
32.8g固体混合物中氯化钠质量为:32.8g-20.8g=12g 答:32.8g固体混合物中氯化钡为20.8g和氯化钠的质量为12g. 故答案为:(1)①920g ②10:39(2)氯化钡为20.8g氯化钠的质量为12g 点评:利用产生沉淀的质量与加入稀硫酸的质量的关系图中折点,读出此时所加稀硫酸恰好完全反应,找出参加反应硫酸的质量,是解决问题的起点.  
练习册系列答案
相关习题
科目:初中化学 来源: 题型:阅读理解  某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题. 某校化学课外活动小组的同学需要一些硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图.请阅读标签上的说明,回答下列问题.(1)打开装有浓硫酸的试剂瓶一段时间后,其溶液的质量会增加,溶质质量分数会 减少 减少 (填“增大”或“减小”)是因为浓硫酸具有吸水 吸水 性.(2)稀释浓硫酸时,正确的操作是 A A (填选项)A.将浓硫酸慢慢倒入盛水的烧杯中,并用玻璃棒不断搅拌 B.将水倒入盛浓硫酸的烧杯中,并用玻璃棒不断搅拌 (3)硫酸的相对分子质量是 98 98 ,硫酸中硫元素与氧元素的质量比为1:2 1:2 (4)取这种浓硫酸50mL,配制成浓度为19.6%的稀硫酸,需要加水多少克? (5)课外活动小组的同学用19.6%的稀硫酸与铜锌合金反应,测定铜锌合金中锌的质量分数,实验数据如表所示:
查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解  现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算: 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
查看答案和解析>> 科目:初中化学 来源: 题型: 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示。请根据有关信息计算: ⑴该试剂中硫酸溶液的质量是 ▲ g。工人小李用该浓硫酸配制20%的稀硫酸,以清洗钢铁表面的铁锈。他在配制该溶液时所用98%的浓硫酸与水的质量比应该为 ▲ 。 ⑵某固体物质由氯化钠和氯化钡混合组成,取32.8g该固体混合物完全溶于水,并逐滴加入上述20%的稀硫,产生沉淀的质量与加入稀硫酸的质量有如下图所示关系,计算32.8g固体混合物中氯化钡和氯化钠的质量。 ⑶若加入的稀硫酸刚好使沉淀最大量时,将所得混合物过滤、洗涤,得滤液200g(过程中损耗忽略不计),计算该滤液中溶质HCl的质量分数。(若溶液中含有多种溶质,则某溶质的质量分数为该溶质的质量与溶液总 质量之比)(反应的方程是为:BaCl2 + H2SO4 = BaSO4↓ + 2HCl)
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |