
| A. | 铁在氧气中燃烧,火星四射,生成红色固体 | |
| B. | 甲烷在空气中燃烧,产生蓝色火焰,生成二氧化碳和水 | |
| C. | 氢氧化钙溶液加入到碳酸钠溶液中,产生红褐色沉淀 | |
| D. | 一氧化碳通过灼热的氧化铁,红棕色固体变为黑色固体 |
分析 A、根据铁丝在氧气中燃烧的现象进行分析判断.
B、根据甲烷在空气中燃烧的现象,进行分析判断.
C、根据盐的化学性质,进行分析判断.
D、根据一氧化碳的化学性质,进行分析判断.
解答 解:A、铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体,故选项说法错误.
B、甲烷在空气中燃烧,产生蓝色火焰,生成二氧化碳和水是实验结论而不是实验现象,故选项说法错误.
C、氢氧化钙溶液加入到碳酸钠溶液中,生成碳酸钙白色沉淀,会观察到产生白色沉淀,故选项说法错误.
D、一氧化碳通过灼热的氧化铁,生成铁和二氧化碳,红棕色固体变为黑色固体,故选项说法正确.
故选:D.
点评 本题难度不大,掌握盐的化学性质、一氧化碳的化学性质、常见物质燃烧的现象即可正确解答,在描述实验现象时,需要注意实验结论和实验现象的区别.


 阶梯计算系列答案
阶梯计算系列答案科目:初中化学 来源: 题型:选择题
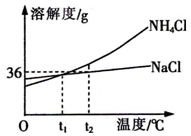
| A. | t1℃时,NaCl和NH4C1两种物质各自的溶液中,所含溶质的质量分数相等 | |
| B. | t2℃时,NH4Cl的溶解度大于NaCl的溶解度 | |
| C. | t2℃时,向18g NaCl固体中加入50g水,充分搅拌后固体能全部溶解,形成氯化钠的饱和溶液 | |
| D. | NH4Cl中含有少量NaCl,可以用冷却热饱和溶液的方法提纯NH4Cl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | 氯化钠 | 35.7 | 36.0 | 37.3 | 38.4 | 39.8 | 39.8 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 现 象 | 结 论 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
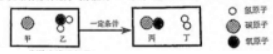 “煤的气化”是指将煤转化为气体燃料-水煤气,有关反应的微观本质如图所示:下列有关该反应的说法错误的是( )
“煤的气化”是指将煤转化为气体燃料-水煤气,有关反应的微观本质如图所示:下列有关该反应的说法错误的是( )| A. | 煤是不可再生能源 | B. | 该反应属于置换反应 | ||
| C. | 图中只有一种氧化物 | D. | 反应中乙、丙的质量比是9:14 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com