
分析 根据物质的化学式可以计算组成元素的质量比;
铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气;
反应前后的质量差即为反应生成氢气的质量,根据氢气的质量可以计算锌的质量、反应的硫酸质量,进一步可以计算弹壳中铜的质量和反应前稀硫酸中溶质的质量分数.
解答 解:(1)Cu2O中铜元素与氧元素的质量比是:(64×2):(16×1)=8:1.
故填:8:1.
(2)设锌的质量为x,反应的硫酸质量为y,
反应生成氢气的质量为:22g+100g-121.8g=0.2g,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.2g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.2g}$,
x=6.5g,y=9.8g,
弹壳中铜的质量为:22g-6.5g=15.5g,
反应前稀硫酸中溶质的质量分数为:$\frac{9.8g}{100g}$×100%=9.8%,
答:生成了0.2g氢气,铜的质量是15.5g,稀硫酸的质量分数是9.8%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:初中化学 来源: 题型:选择题
| A. | 加热后的试管立即用冷水冲洗 | |
| B. | 实验用剩的药品放回原试剂瓶中 | |
| C. | 向试管中滴加液体时,胶头滴管垂悬在试管口上方,不接触试管 | |
| D. | 为了便于观察,给试管里的液体加热时试管口对着自己 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 蜡烛的着火点较低 | |
| B. | 空气流动使蜡烛接触的氧气减少 | |
| C. | 降低了蜡烛的着火点 | |
| D. | 空气流动带走燃烧的热量使烛火的温度低于蜡烛的着火点 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
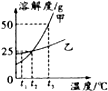
| A. | 甲中混有少量乙时,提纯甲的方法是降温结晶 | |
| B. | 甲、乙物质的溶解度都为25g | |
| C. | t3℃,在150g水中加入80g甲物质,得到溶液的质量为225g | |
| D. | 将t3℃时等质量的甲、乙饱和溶液分别降温到t1℃,则甲溶液的溶质质量分数小于乙 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com