
(8分)化学实验是学习化学的基础,请根据下列装置图回答问题。


A B C
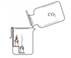
(1) A实验:把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有 、 和 的性质,因此二氧化碳在实际生活中可用于灭火。
(2) B实验:有关反应的化学方程式为 ;烧杯中热水的作用是使白磷与空气隔绝和 ;通过该实验可得出燃烧需要三个条件:①可燃物②可燃物与 接触③温度达到 的结论。
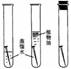
(3) C实验:试管③实验的目的是探究铁钉在 的情况下是否生锈;试管①中的铁钉与水面接触的一圈最容易生锈,其原因是___________。
(1)(共2分)不能燃烧、也不支持燃烧 ,密度比空气大(答对两空给1分,答对三空给2分)
(2)4P
+ 5O2 2P2O5 升高温度达到白磷的着火点
2P2O5 升高温度达到白磷的着火点
空气(或氧气) 燃烧所需的最低温度(或着火点)
(3)没有水(或只与空气接触) 该部位既与水接触又与空气(或氧气)接触
【解析】
试题分析:(1)根据蜡烛由下到上依次熄灭来推断二氧化碳的性质,既要考虑物理性质,又要考虑化学性质,故把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有密度比空气大、不燃烧和不支持燃烧的性质。
(2)白磷燃烧生成五氧化二磷,故反应的化学方程式为4P + 5O2 2P2O5;
2P2O5;
根据燃烧的条件,结合图示可知,烧杯中的热水的作用是使白磷与空气隔绝和升高温度达到白磷的着火点;
通过该实验可得出,燃烧需要同时满足三个条件:①可燃物,②与氧气接触,③温度达到着火点,三个条件缺一不可。
(3)根据铁生锈的条件分析,铁生锈是铁与氧气和水共同作用的结果,试管③中的铁钉存放在干燥的空气中,故实验的目的是探究铁钉在没有水的情况下是否生锈;试管①中的铁钉与水面接触的一圈最容易生锈,其原因是该部位既与水接触又与空气(或氧气)接触。
考点:探究二氧化碳的性质,探究金属锈蚀的条件,燃烧的条件与灭火原理探究,书写化学方程式,燃烧与燃烧的条件
点评:要想解答好这类题目,就要理解和熟记燃烧与燃烧的条件,以及生锈的条件,再根据所给的实验、问题情景等,结合所学的相关知识和技能,以及自己的生活经验所得,细致地分析题意,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
(8分)
碳酸钙可用于预防和治疗钙缺乏症。某实验小组同学要测定一种钙片中碳酸钙的含量。
【查阅资料】获得的资料有:
补钙剂中常加入糖类、维生素D等改善口感或增强药效。这些物质不与稀盐酸反应产生气体,高温灼烧时会燃烧或分解。
碳酸钙高温灼烧分解生成氧化钙和二氧化碳。
常见的碳酸钙含量测定方法:将碳酸钙粉碎,加入已知浓度的过量盐酸充分反应,然后测剩余盐酸的量,根据消耗盐酸的量最终求得碳酸钙的含量。
澄清石灰水中的Ca(OH)2含量很少,100 g澄清石灰水中最多含0.15 g Ca(OH)2。
【方案设计和实施】根据资料和已学知识,该小组同学设计如下两种方案进行测定。
方案1:根据下图所示装置实验。

(1)锥形瓶中发生反应的化学方程式为 。
(2)长颈漏斗下部插入液面下的目的是 。
(3)加入药品前,检验该装置气密性的方法是 。
(4)记录数据如下:
| 钙片质量 | 空洗气瓶质量 | 澄清石灰水的质量 | 反应后洗气瓶及瓶内物质总质量 |
| 25 g | 100 g | 200 g | 300.4 g |
方案2:将钙片粉碎,加入足量的稀盐酸充分反应,根据放出气体的量计算碳酸钙的含量。记录数据如下(空烧杯质量为100 g,加入钙片质量为25 g):
| 加入稀盐酸的质量 | 100 g | 200 g | 300 g | 400 g |
| 充分反应后烧杯及杯内物质总质量 | 222.8 g | 320.6 g | 418.4 g | 518.4 g |
【分析和评价】
(1)方案1和方案2中合理的是 ,原因是 。
(2)该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是 。
(3)要使用【查阅资料】(3)中介绍的方法,还需要学习的是 。
【结论】经过计算,该钙片中碳酸钙的质量分数是 。
查看答案和解析>>
科目:初中化学 来源:2012届江苏省苏州市景范中学初三中考二模化学试卷(带解析) 题型:填空题
(8分)对碳酸钙、碳酸氢铵、碱式碳酸铜三种碳酸盐的性质比较:
在1、2、3三试管中依次加入碳酸钙、碳酸氢铵、碱式碳酸铜各少量固体(各2份)。
第一份:在1、2、3三试管中各倒入少些水并振荡至充分溶解,用玻璃棒蘸取液体并与标准比色卡对照,可测定三种物质的pH 。实验时要多次使用玻璃棒,所以,每次测定后应对玻璃棒进行 处理。根据你的实验结果,可以得出上述三种碳酸盐水溶液的pH由大到小的顺序是(填试管编号):
试管 >试管 >试管 。(1分)
将1、2、3三试管置于烧杯内热水水浴。根据你的实验结果和学过的知识,可以得出
三种碳酸盐的热稳定性由强至弱的顺序是(填化学式):
> > 。(1分)
按盐的组成分类,碳酸钙、碳酸氢铵、碱式碳酸铜依次为正盐、酸式盐和碱式盐。初步推想,正盐、酸式盐和碱式盐的热稳定性由强至弱的顺序应该是:
> > 。(1分)
第二份:在1、2、3三试管中分别加入稀盐酸,都能观察到 。
要鉴定该气体,你的操作方法是: 。
碳酸钙和适量稀盐酸反应至气泡逸出不明显后,测得其残留液pH等于2。 此时取适量
反应后溶液,逐滴滴入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如下[ pH为纵坐标,时间s(秒)为横坐标]: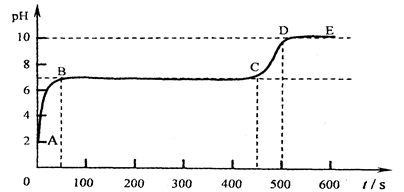
①写出BC“平台”段化学方程式 ;
②CD段上升的原因是: 。
查看答案和解析>>
科目:初中化学 来源:2008届北京市怀柔区中考二模化学试卷(解析版) 题型:填空题
(8分)我国劳动人民早在春秋战国时期就已经懂得钢铁冶炼,铁也是生活中使用最为广泛的金属,目前我国钢铁产量已经位居世界第一。下面是一组有关铁的问题,请你用所学化学知识加以回答:
(1)用赤铁矿(Fe2O3)炼铁的化学反应方程式是 。成语“千锤百炼”就源于生铁炼钢的过程,该过程中发生化学反应的化学方程式是 。
(2)铁可以拉成铁丝,压成铁片,这是利用了铁的 性;在公路上行驶的油罐车尾部经常有一条铁链拖在地面上,这是利用了铁的 性;家里铁制炊具要有木柄或塑料柄,这是因为铁有很好的 性;
(3)焊接钢管时,经常用硫酸铜溶液在钢管表面画交叉线,然后根据出现的红线对准焊接,用化学方程式表示反应原理 。
(4)经研究发现,长期使用我国发明的铁锅炒菜做饭,可有效地减少缺铁性贫血的发生,如果在炒菜时经常加入适量的食用醋,效果会更好,理由是_________________ 。
(5)某同学在做盐酸和锈铁钉反应实验时,发现含锈的铁钉表面出现了气泡,你觉得原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com